Электролитные нарушения, в частности гипокалиемия, являются одними из этиологических факторов рабдомиолиза. В статье представлено пять клинических случаев гипокалиемического рабдомиолиза. Диагностический поиск, включая ультразвуковое исследование мышц, позволил своевременно поставить правильный диагноз и провести комплексную терапию.
Введение. Рабдомиолиз (РМ) представляет собой клинико-лабораторный синдром, развивающийся при повреждении скелетных мышц и выброса в системный кровоток потенциально токсичных веществ. Тяжесть РМ варьирует от бессимптомного течения (диагностируется на основании повышения в крови уровня мышечных ферментов) до развития полиорганной недостаточности с превалированием острого повреждения почек (ОПП).
Традиционно РМ ассоциирует с травмами или реперфузионными нарушениями. Однако, существует большая группа заболеваний, приводящих к РМ без видимой деструкции мышц. Нарушения электролитного баланса, такие как гипонатриемия, гипокалиемия и гипофосфатемия, – один из этиологических факторов РМ [1].
Гипокалиемия, возникающая при целом ряде патологических состояний, наиболее частая причина развития РМ среди электролитных нарушений. Традиционно потери калия ассоциируются с патологией желудочно-кишечного тракта. Обычно это связано с длительной диареей или рвотой, кишечной непроходимостью или инфекциями [2].
Лекарственные препараты, такие как инсулин, диуретики, слабительные и антибиотики пенициллинового ряда, производные ксантина (теофиллин, кофеин) также могут быть причиной гипокалиемии [2,3]. Клинически значимая гипакалиемия наблюдается при дефиците магния, особенно связанного с приёмом петлевых или тиазидных диуретикров [4].
Солодка является растительным компонентом, входящим в состав сладостей, напитков, а также отхаркивающих, противовоспалительных средств и травяных сборов. Развитие РМ в случае передозировки солодкой связано с подавлением 11-β-гидроксистероид дегидрогеназы типа 2. Это вызывает гипокалиемию, метаболический алколоз, мышечную слабость и нарушение дыхания. В тяжелых случаях развивается РМ [5,6].
Группа эндокринных заболеваний, в которую входят первичный (болезнь Кона), вторичный гиперальдостеронизм и ренин-индуцированные опухоли почек вызывают гипокалиемическую миопатию. В основе развития гипокалиемии при этих заболеваниях лежит повышенная экскреция калия в связи с резистентностью почечных канальцев к альдостерону [7].
При сахарном диабете, в частности диабетическом кетоацидозе, причиной гипокалиемии являются дефицит инсулина, повышенная почечная экскреция калия и истощение его запасов в тканях.
Патология почек и нарушение функции почечных канальцев приводят к гипокалиемии. В первую очередь к данной патологии следует отнести синдром Олбрайт-Лайтвуда, синдром Фанкони и нефрит.
Гипокалиемия - лабораторный маркер синдрома Гительмана, который наследуется как аутосомно-рецессивный признак и является одним из наиболее частых наследственных заболеваний почечных канальцев с частотой 1 на 40 тыс. населения у представителей европеоидной расы. Причиной синдрома Гительмана являются инактивирующие мутации в гене NCC (SLC12A3), которые приводят к тиазидоподобному эффекту, заключающемуся в потере ионов натрия и хлора со вторичной гиповолемией и последующей стимуляцией системы ренин-ангиотензин-альдостерон [7,8].
В основе патогенеза гипокалиемического РМ лежит деполяризация мышечной мембраны в результате нарушения работы Na+-K+ насоса, подавление продукции и хранения гликогена в миоцитах и нарушение микроциркуляции [1].
Тяжесть клинических проявлений гипокалиемии, как правило, пропорциональна степени и продолжительности снижения уровня калия в сыворотке крови. Клинические симптомы обычно не проявляются до тех пор, пока уровень калия в сыворотке крови не снизится до 3,0 ммоль/л. Характерны нарушения ритма сердца вплоть до развития жизнеугрожающих состояний [9].
Типичными жалобами больных с гипокалиемией являются утомляемость, мышечные спазмы и мышечная слабость. Как правило, мышечная слабость возникает в нижних конечностях и впоследствии распространяется на туловище и руки. Нарушения перистальтики кишечника и обстипация – могут свидетельствовать о тяжёлой гипокалиемии.
Признаками гипокалиемии на электрокардиограмме (ЭКГ) являются появление зубцов U, уплощение зубца Т и изменения сегмента ST, сердечные аритмии.
Маркёрами РМ считают креатинфосфокиназу (КФК) и миоглобин (МГ), которые повышаются в сыворотке крови вследствие повреждения миоцитов. Превышение концентрации КФК 5000 ед/л является неблагоприятным предиктором развития ОПП [11,12].
При ультразвуковом исследовании (УЗИ) в В-режиме при РМ может быть выявлено: наличие чередующихся участков повышенной и пониженной эхогенности в структуре мышц в острой фазе мышечного повреждения, снижение либо повышение эхогенности мышечных волокон, вызванное отёком и воспалением мышц, дезорганизация их фасцикулярной архитектоники, представляющей собой участки некроза, наличие жидкостных включений, увеличение толщины мышц [12]. В последние годы для оценки структурных изменений мышц стали использоваться такие УЗ методики, как компрессионная эластография (ЭГ) и ЭГ сдвиговой волны, позволяющие произвести оценку как качественных, так и количественных показателей плотности мышц, определить эластичность/плотность мышечной ткани.
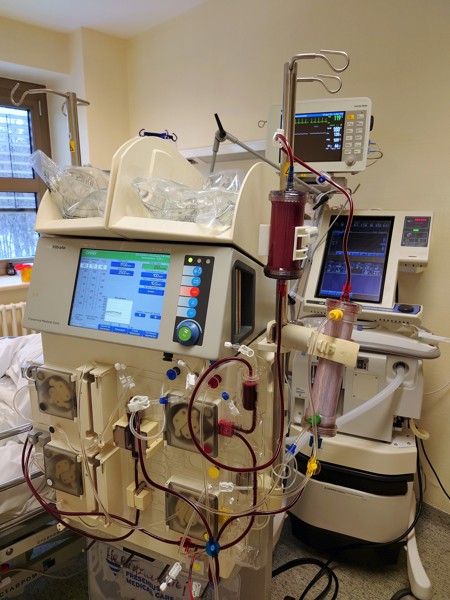
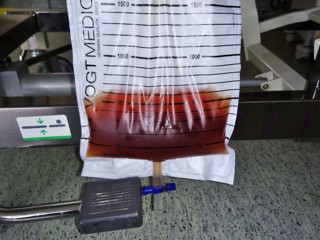
При лечении гипокалиемического РМ необходимо нормализовать водно-электролитный баланс и уровень калия в плазме крови. Кроме того, следует предупредить развитие вторичных осложнений, в первую очередь ОПП. С целью быстрой элиминации МГ и профилактики/лечения ОПП применяют экстракорпоральные методы детоксикации (ЭМД), такие как сорбция, плазмообмен (ПО), гемодиафильтрация (ГДФ) и гемодиализ [12].
В своей клинической практике мы наблюдали 5 случаев гипокалиемического РМ.
Случай 1. Больной 89 лет госпитализирован в стационар с жалобами на слабость в конечностях, в шее, осиплость голоса, невозможность держать голову. В анамнезе ишемическая болезнь сердца (ИБС), гипертоническая болезнь (ГБ), длительный приём мочегонных препаратов. В лабораторных анализах: К+ 1,24 ммоль/л (референсные значения 3,70-5,50 ммоль/л), Na 149 ммоль/л (референсные значения 135-152 ммоль/л), креатинин 183 мкмоль/л (референсные значения 62-106 мкмоль/л), КФК 30594 ед/л (референсные значения 39-308 ед/л), МГ 9618 нг/мл (референсные значения 23,0-72,0 нг/мл). На ЭКГ зафиксирована предсердная и желудочковая экстрасистолии, удлинение интервала QTс более 500 мс, депрессия ST в отведениях V2-5. При УЗИ в В-режиме определялось диффузное снижение эхогенности утолщенных мышц, смазанность рисунка мышц, межфасциальный отек. При компрессионной ЭГ в структуре мышечного волокна определялись высокоэластичные зоны, при ЭГ сдвиговой волны плотность мышц была снижена и составила 1,4 м/с (референсное значение величины плотности мышечной ткани у мужчин 2,79-2,91 м/с, у женщин – 1,73-2,56 м/с) [13]. Состояние расценено как гипокалиемический РМ. Терапия включала коррекцию водно-электролитных нарушений, проведения сеанса сорбции CytoSorb®.
Случай 2. Больной 74 лет госпитализирован в стационар с жалобами на онемение в руках и ногах, боли в мышцах. В анамнезе ИБС, ГБ, сахарный диабет (СД), первичный гипотиреоз, хроническая обструктивная болезнь лёгких, приём отхаркивающих микстур. В лабораторных анализах: К+ 2,1 моль/л, Na+ 140 ммоль/л, креатинин 634 мкмоль/л, КФК 7872 ед/л, МГ 3511 нг/мл. На ЭКГ частые предсердные экстрасистолы, удлинение интервала QTс. При УЗИ в В-режиме определялось умеренное диффузное снижение эхогенности промежуточной мышцы бедра, снижение структурности мышц с наличием межмышечно расположенных анэхогенных зон округлой формы (очагов миолиза). При компрессионной ЭГ мышцы характеризовались равномерным эластичным окрашиванием с наличием высокоэластичных зон, при ЭГ сдвиговой волны плотность мышц составила 1,73 м/с Состояние расценено как гипокалиемический РМ. Терапия включала коррекцию водно-электролитных нарушений, в связи с развитием у больного РМ ассоциированного ОПП стадия F по шкале RIFLE проведено 4 сеанса ГДФ в комбинации с сорбцией CytoSorb®.
Случай 3. Больная 71 года госпитализирована в стационар с жалобами на слабость, тошноту, частый жидкий стул, эпизоды гипотонии на фоне приёма гипотензивных препаратов. В анамнезе ГБ. В лабораторных анализах: K+ 2,73 моль/л, Na+ 103 ммоль/л, креатинин 49 мкмоль/л, КФК 4601 ед/л, МГ 1018 нг/мл. На ЭКГ ишемические изменения миокарда передне-распространённых отделов левого желудочка, удлинение интервала QTс до 490 мс. При УЗИ в В-режиме определялись смазанность рисунка утолщенных мышц, умеренное диффузное снижение эхогенности, межмышечно визуализировались гипоэхогенные зоны с размытыми контурами. При компрессионной ЭГ мышцы характеризовались эластичным окрашиванием с наличием высокоэластичных зон, при ЭГ сдвиговой волны плотность мышц составила 1,17 м/с. Состояние расценено как гипокалиемический РМ. В связи с тяжёлыми водно-электролитными нарушениями, включая гипонатриемию, в интенсивную терапию включена ГДФ и ПО.
Случай 4. Больная 74 лет госпитализирована в стационар с жалобами на слабость, нарушение походки, эпизоды гипотонии на фоне гипотензивной терапии. В анамнезе ИБС, ГБ, СД, цереброваскулярная болезнь. В лабораторных анализах: К+ 3,14 моль/л, Na+ 140 ммоль/л, креатинин 290 мкмоль/л, КФК 1225 ед/л, МГ 721 нг/мл. На ЭКГ предсердная экстрасистолия. При УЗИ в В-режиме определялись смазанность рисунка утолщенных мышц с аркоподобными выбуханиями фасций, наличие в структуре мышц участков повышенной эхогенности с размытыми контурами по типу «матового стекла». При компрессионной ЭГ мышцы характеризовались эластичным окрашиванием с наличием высокоэластичных зон, при ЭГ сдвиговой волны плотность мышц составила 1,27 м/с. Терапия включала коррекцию водно-электролитных нарушений.
Случай 5. Больной 77 лет госпитализирован в стационар вследствие острой экзогенной интоксикации неустановленным веществом (вероятно, суррогатами алкоголя). По тяжести состояния больной активных жалоб не предъявлял. В лабораторных анализах: K+ 2,88 ммоль/л, Na+ 147 ммоль/л, креатинин 355 мкмоль/л, КФК 1161 ед/л, МГ 1669 нг/мл. На ЭКГ фибрилляция предсердий. При УЗИ в В-режиме определялись смазанность рисунка мышц, незначительное повышение эхогенности. При компрессионной ЭГ мышцы характеризовались эластичным окрашиванием с наличием высокоэластичных зон, при ЭГ сдвиговой волны плотность мышц составила 1,25 м/с. В связи с ОПП стадия F по RIFLE выполнено 2 сеанса ГДФ в комбинации с сорбцией CytoSorb®.
Обсуждение. РМ – полиэтиологическое заболевание. Нередко нетравматические факторы имеют ведущее значение в его развитии. Применение лекарственных препаратов, например диуретиков у больных с сердечно-сосудистыми заболеваниями, могут провоцировать водно-электролитные нарушения, включая гипокалиемию. Ещё одной причиной РМ, связанного фармакотерапией, являются препараты растительного происхождения для подавления кашля на основе корня солодки, которые без рецептов продаются в аптечной сети [1,2,3].
В представленном нами клиническом наблюдении все больные были старшей возрастной группы с тяжёлой коморбидной патологией, включая сердечно-сосудистые заболевания. Этиологическими причинами являлись длительный приём диуретиков (3 больных) и препаратов от кашля, в состав которых входил корень солодки (1 больной), экзогенная интоксикация (1 больной).
В клинико-лабораторной картине наблюдались гипокалиемия, повышение концентрации КФК в плазме крови и признаки ОПП. Учитывая высокие значения КФК при отсутствии видимых повреждений мышц, нами был выполнен диагностический поиск, который включал определение МГ в сыворотке крови и УЗ-исследование 4-х главой мышцы бедра. Уровень МГ превышал референсные значения от 9 до 128 раз.
При УЗИ во всех случаях определялись стёртость мышечного рисунка, изменения эхогенности и неоднородность структуры мышц, снижение плотности мышц по данным методик компрессионной ЭГ и ЭГ сдвиговой волны. С учетом полученных данных всем больным установлен диагноз гипокалиемического РМ.
Интенсивная терапия включала инфузионную терапию, направленную на достижение нормоволемии, коррекцию водно-электролитных нарушений и кислотно-основного состояния.
Несмотря на то, что в настоящее время не существует клинических рекомендаций применения ЭМД у больных РМ, данные методы необходимо активно применять с целью элиминации продуктов цитолиза, эндогенной интоксикации, образующихся в результате повреждения и некроза мышц. Четырём больным дополнительно были проведены сеансы ЭМД. На фоне комплексной интенсивной терапии удалось компенсировать электролитные нарушения, предупредить или купировать проявления РМ-ассоциированного ОПП.
В представленных клинических наблюдениях нами использован комплексный подход в диагностике и лечении больных нетравматическим РМ. Правильно собранный анамнез, данный клинико-лабораторной картины позволили заподозрить РМ у больных с гипокалиеией. Подтвердить наше предположение удалось с помощью ультразвуковой диагностики при выявлении изменений мышц, характерных для РМ.
Заключение. В клинической практике последних лет увеличилась встречаемость случаев нетравматического РМ. Однако, у врачей нет настороженности в отношении этой патологии и часто она остается либо вовсе не распознанной, либо ее начинают лечить на стадии развития ОПП. Использование методов УЗИ-диагностики позволяет своевременно выявить РМ и начать лечении этого патологического состояния.
Список литературы.
- Huerta-Alardín A.L., Varon J., Marik P.E. Bench-to-bedside review: Rhabdomyolysis – an overview for clinicians. Critical Care. 2005; 9: 158-169 doi: 10.1186/cc2978.
- Kardalas E., Paschou S.A., Anagnostis P., Muscogiuri G., Siasos G., Vryonidou A. Hypokalemia: a clinical update. Endocr Connect. 2018; 7(4): R135-R146.doi: 10.1530/EC-18-0109.
- Ruisz W., Stöllberger C., Finsterer J., Weidinger F. Furosemide-induced severe hypokalemia with rhabdomyolysis without cardiac arrest. BMC Womens Health. 2013; 13: 30. doi: 10.1186/1472-6874-13-30.
- Clausen T. Hormonal and pharmacological modification of plasmapotassium homeostasis. Fundam Clin Pharmacol. 2010; 24(5): 595-605. doi: 10.1111/j.1472-8206.2010.00859.x.
- Omar H.R., Komarova I., El-Ghonemi M. et al. Licorice abuse: time to send a warning message. Ther Adv Endocrinol Metab. 2012; 3(4): 125-138. doi: 10.1177/2042018812454322.
- McHugh J., Nagabathula R., Kyithar M.P. A life-threatening case of pseudo-aldosteronism secondary to excessive liquorice ingestion. BMC Endocr Disord. 2021; 21(1): 158. doi: 10.1186/s12902-021-00816-4.
- Pecnik P., Müller P., Vrabel S., Windpessl M. Two cases of hypokalaemic rhabdomyolysis: same but different. BMJ Case Rep. 2018; 2018: bcr2017223609. doi: 10.1136/bcr-2017-223609.
- Blanchard A., Bockenhauer D., Bolignano D., Calò L.A., Cosyns E., Devuyst O., Ellison D.H., Karet Frankl F.E., Knoers N.V., Konrad M., Lin S.H., Vargas-Poussou R. Gitelman syndrome: consensus and guidance from a Kidney Disease: Improving Global Outcomes (KDIGO) Controversies Conference. Kidney Int. 2017; 91(1): 24-33. doi: 10.1016/j.kint.2016.09.046.
- Tran T.T.T., Pease A., Wood A.J., Zajac J.D., Mårtensson J., Bellomo R., Ekinci E.I.I. Review of Evidence for Adult Diabetic Ketoacidosis Management Protocols. Front Endocrinol (Lausanne). 2017; 8: 106. doi: 10.3389/fendo.2017.00106.
- Zacchia M., Abategiovanni M.L., Stratigis S., Capasso G. Potassium: From Physiology to Clinical Implications. Kidney Dis (Basel). 2016; 2(2): 72-79. doi: 10.1159/000446268.
- Brown C, Rhee P, Chan L, Evans K, Demetriades D, Velmahos G. Preventing renal failure in patients with rhabdomyolysis: do bicarbonate and mannitol make a difference? J Trauma. 2004; 56: 1191-1196. doi: 10.1097/01.ta.0000130761.78627.10.
- Фёдорова А.А., Кутепов Д.Е., Зубарев А.В., Пасечник И.Н., Хабарина Н.В. Рабдомиолиз: что нового в диагностике и лечении? Кремлевская медицина. Клинический вестник. 2020; 2: 103-110. doi: 10.26269/4n94-0746.
- Делягин В.М. Ультразвуковое исследование мышц в норме и при нейромышечной патологии. Sonoace Ultrasound. 2015; 27: 68-73.
10 августа 2023 г.
Ещё больше полезной информации на нашем Телеграм-канале