В настоящее время методы эндоскопического гемостаза играют важную (но не исключительную) роль в лечении больных с ОГДЯК. Само внедрение в клиническую практику эндогемостаза помогло избежать большого числа экстренных операций, позволив принципиально иначе взглянуть на необходимость оперативного лечения многих пациентов с ОГДЯК или, как минимум, дав возможность отсроченного проведения операции после соответствующей подготовки больных.
К сегодняшнему дню предложено более пятидесяти методик эндоскопической остановки кровотечения, практически ежегодно появляются новые или модифицируются прежние способы воздействия на источник кровотечения в гастродуоденальных язвах. Несмотря на все многообразие способов эндогемостаза и наличие более или менее конкретных показаний к применению каждого, в конкретной клинике, как правило, используется не более двух или трех определенных методик. Это связано не столько с известным консерватизмом и приверженностью традициям, сколько с крайне ограниченными материальными возможностями стационаров. Но, как показывает практика, даже самые современные средства эндогемостаза нередко вызывают у клиницистов досаду и разочарование вследствие возникшего рецидива кровотечения. И это связано не с несовершенством методики или техники выполнения процедуры, а с некорректной постановкой задачи и, соответственно, с неадекватностью ожидаемого от эндогемостаза результата имеющимся реалиям патолгического процесса. Глубоким заблуждением, например, будет ожидание стабильного гемостаза после любых эндоскопических манипуляций при кровотечении Forrest Ia из каллезной язвы малой кривизны желудка. Оценка потенциальных возможностей эндоскопической остановки кровотечения в плане достижения стабильного гемостаза в каждой конкретной ситуации должна проводиться отдельно, и зависит, прежде всего, от объективно установленной вероятности развития рецидива кровотечения, а не от применявшегося метода эндогемостаза. Несмотря на отдельные сообщения об успешном внедрении того или иного нового метода эндогемостаза в клиническую практику, принципиального изменения стратегии ведения больных с ОГДЯК не происходит: по-прежнему достаточно часто пациенты оперируются в экстренном и срочном порядке в связи с нестабильным гемостазом и рецидивом кровотечения. Поэтому эндоскописту и, тем более, хирургу следует a priori сдержанно относиться к самой возможности достижения окончательного гемостаза при язвенном кровотечении и скрупулезно оценить все прогностически неблагоприятные факторы возникновения рецидивной геморрагии вне зависимости от способа предполагаемого или проведенного эндогемостаза.
К эндоскопическому оборудованию, применяемому для проведения гемостаза при ОГДЯК предъявляется ряд специфических требований. Ю. М. Панцырев и Ю. И. Галлингер (1984) указывают, что для эндоскопических манипуляций при ОГДЯК предпочтительно использование эндоскопов с широким инструментальным каналом (3, 7 мм), что облегчает и ускоряет аспирацию содержимого желудка. При массивных кровотечениях более удобен для манипуляций эндоскоп с двумя инструментальными каналами, поскольку в данном случае имеется возможность струйного прицельного промывания источника кровотечения через катетер, проведенный через один инструментальный канал, и одновременных манипуляций инъектором или зондом для электрокоагуляции, проведенными через другой инструментальный канал. Эти же авторы рекомендуют при кровотечении из язв малой кривизны желудка применять эндоскопы с боковой оптикой. Мы считаем возможным использование при ОГДЯК эндоскопов с торцевой оптикой и диаметром инструментального канала 2, 8 мм, поскольку в современной клинической практике доступен к использованию практически весь спектр инструментов, подходящих для эндоскопов с каналом данной величины.
Весь современный арсенал средств эндоскопической остановки кровотечения и превентивного эндоскопического гемостаза принято разделять на три основные группы в зависимости от основного действующего фактора: методы медикаментозного воздействия, методы механического воздействия и методы физического воздействия.
Методы медикаментозного воздействия в зависимости от способа введения фармакологического агента подразделяются на орошение язвенной поверхности, аппликацию пленкообразующих полимеров на язвенную поверхность, инфильтрацию ткани язвенного кратера и периульцерозной зоны.
Орошение язвенной поверхности проводится либо с целью ускорения образования кровяного сгустка и тромба на кровоточащей поверхности язвенного кратера, либо для индукции стойкого спазма артерий в ткани язвы, либо для поверхностной денатурации тканевых белков дна язвенного кратера. Орошение язвенной поверхности pаствоpами лекарственных средств повеpхности пpоводится прицельно под контролем зрения с помощью специальных pаспыляющих катетеpов типа PW-6С-1 (Olympus) или с помощью обычного катетеpа. В качестве средств, активирующих локальное тромбообразование (местные гемостатики) целесообразно использовать:
- Капрофер – карбонильный комплекс треххлористого железа с аминокапроновой кислотой на физиологическом растворе. Механизм гемостатического эффекта капрофера основан на химической коагуляции гема треххлористым железом, повышении активности тканевого тромбопластина. Капрофер способствует формированию и организации кровяного сгустка, который плотно фиксируется на раневой поверхности и тем самым предупреждает повторное кровотечение. Препарат ускоряет регенерацию и послеоперационную эпителизацию раневой поверхности, образование грануляционной ткани; оказывает противовоспалительное, противоотечное, антиоксидантное, антисептическое и противогрибковое действие.
- Феракрил (1% раствор) - неполная железная соль полиакриловой кислоты, образует нерастворимый сгусток с белками крови (в первую очередь с альбумином) на поверхности язвы и тем самым оказывает местное гемостатическое действие. Кровотечение из мелких сосудов при применении феракрила прекращается через 1–2 мин. Препарат обладает местноанестезирующим эффектом и умеренной антибактериальной активностью.
- ε – аминокапроновая кислота (5% и 20% раствор) – местный и системный гемостатик, в основе действия которого находится инактивация фибринолиза за счет блока активаторов плазминогена.
Для индукции сосудистого спазма в поверхностных слоях ткани язвенного кратера следует применять адреномиметики адреналин (1% раствор) , мезатон (1 % раствор) . Для денатурации тканевых белков на поверхности дна язвы используется 96% этиловый спирт.
Следует отметить, что в качестве самостоятельного метода эндогемостаза оpошение язвенной поверхности используют редко – только пpи малоинтенсивных паpенхиматозных кpовотечениях или при спонтанном гемостазе (Forrest IIb-IIc) для пpофилактики pецидива кpовотечения. Как правило, орошение язвенной поверхности является компонентом комбинированных методов эндогемостаза.
Аппликация пленкообразующих полимеров на язвенную поверхность имеет к настоящему моменту уже тридцатилетнюю историю применения и в качестве самостоятельного метода гемостаза не используется ввиду технической сложности применения методики и сравнительно малой ее эффективности. Целью аппликации полимеров на язвенную поверхность является ее защита от кислотно-пептического фактора желудочного сока. Для формирования на язвенном кратере полимерной пленки используют аэрозоли на основе полиметакрилатов (лифузоль, гастрозоль, статизоль) и медицинские клеи на основе цианокрилатов (МК-6, МК-7, МК-8).
Перед нанесением полимера в виде жидкости или аэрозоля на язвенную поверхность последняя тщательно очищается от слизи, крови, элементов пищи интенсивным промыванием водой, а затем высушивается нанесением спирта или эфира. Собственно методика аппликации сводится к следующему. Перед использованием клей МК разводится в соотношении 1: 3 хлорэтилом; через катетер, подведенный к язвенному дефекту клей наносится «сверху вниз»; в катетер сразу же после аппликации клея вводят 1-2 мл хлорэтила; желудок раздувают воздухом для фиксации клея к ткани; извлекают эндоскоп, конец катетера очищают ацетоном и только после этого извлекают из инструментального канала во избежание «пломбировки» последнего. Срок нахождения клеев МК на ткани язвенного кратера – не более суток, клеевых аэрозолей – не более 2 суток, что требует проведения повторных ежедневных аппликаций. Трудоемкость данного метода эндогемостаза и реальная опасность повреждения эндоскопов в сочетании с его малой эффективностью, а также возможность подавления кислотно-пептического фактора антисекреторными средствами обусловили исключительно редкое применение аппликации пленкообразующих препаратов и только в составе комбинированных методов эндогемостаза.
Новые возможности применения аппликаций пленкообразующих препаратов открылись с внедрением в клиническую практику препарата ТахоКомб®, состоящим из коллагеновой пластины, покрытой сухим высоко концентрированным фибриногеном, тромбином и ингибитором фибринолиза апротинином. Для производства ТахоКомба® применяется специальная методика тонкого нанесения фибринового клея. Учитывая, что тромбин мгновенно реагирует с фибриногеном даже в присутствии стабилизатора апротинина, компоненты фибринового покрытия распыляются в органической среде, и данная суспензия накладывается на пластину коллагена. Органическая среда в дальнейшем испаряется, оставляя слой компонентов фибринового клея, абсорбированных на коллагеновой основе. При контакте с тканевыми жидкостями происходит реакция полимеризации фибринового покрытия, а коллаген в течение в среднем 4 минут образует водо- и воздухонепроницаемый слой. Во время этого процесса пластина Тахокомба должна быть плотно прижата к поверхности язвенного кратера. Пластина хорошо адаптируется как к ровным, так и бугристым раневым поверхностям, а механическая стабильность коллагеновой пластины обеспечивает дополнительную защиту ткани язвы. Компоненты ТахоКомб® деградируют в организме под действием ферментов в пределах 3-6 недель. Для достижения эндоскопического гемостаза пластина ТахоКомба® 2, 5 х 3, 0 х 0, 5 см в свернутом состоянии проводником параллельно уже введенному эндоскопу доставляется в желудок. Биопсийными щипцами пластина разворачивается и прижимается к свободному от крови язвенному кратеру на 3 – 5 минут. Применение ТахоКомба® – очевидно перспективный метод эндоскопического гемостаза, однако при ОГДЯК метод требует дальнейших клинических исследований и разработки стандартизованного способа введения в желудок пластины препарата.
Инфильтрация ткани язвы и периульцерозной зоны лекарственными препаратами является самым широко распространенным методом эндоскопического гемостаза. Инъекционный метод может быть применен практически во всех случаях язвенного кровотечения. Абсолютных противопоказаний к его использованию нет, относительным противопоказанием к применению инъекционного метода является диффузный характер поражения слизистой. Механизм инфильтрационного гемостаза заключается в остановке кровотечения за счет гидравлической компрессии сосудов, сосудистого спазма, усиления местного тромбообразования и склероза в непосредственной близости от источника геморрагии, достигаемых перифокальными инъекциями лекарственных препаратов. Для проведения инфильтрационного гемостаза могут быть использованы: 0, 1% раствор адреналина гидрохлорида, 3% раствор NaCl, 70% раствор этилового спирта изолированно или в сочетании с новокаином, масляные растворы, фибриновый клей, цианокрилаты, двухкомпонентные силиконовые композиции, склерозанты, препараты с антиоксидантной активностью.
Для проведения инфильтрационного гемостаза используются металлические или пластиковые эндоскопические инъекторы типа NM – 4 … 7L-1, NM-200L-0421 (производство Olympus) с диаметром 21-23 G (для инструментального канала 2, 8мм) и длиной выдвижной иглы 4 – 6 мм (рис. ). Инъекторы состоят из стерильной одноразовой иглы и автоклавируемого спиралевидного тубуса из нержавеющей стали. Оболочка тубуса снабжена гибкой дистальной трубкой для облегчения ввода в инструментальный канал эндоскопа. Возможно применение инъекторов, в которых вместо металлического тубуса используется тефлоновый катетер, обеспечивающий необходимую гибкость и жесткость, гарантируя безопасный ввод иглы. Тефлоновая оболочка облегчает ввод иглы в подслизистый слой, что делает данный тип инъектора особенно удобным для субмукозных инъекций при эндогемостазе.
Методика проведения инфильтрационного эндогемостаза различается в зависимости от характера источника кровотечения, его интенсивности, вида вводимого препарата.
Для достижения гидравлической компрессии кровоточащих сосудов язвенного кратера игла эндоскопического инъектоpа, проведенная через биопсийный канал эндоскопа, вкалывается на максимальную глубину в пеpиульцеpозной зоне в 2 – 3 мм от источника кровотечения поочередно из 5 – 6 точек. Через инъектор в стенку желудка или ДПК вводится лекарственный препарат в объеме до 50-300 мл до образования отчетливого выбухающего валика вокруг источника кровотечения («инфильтрационный жгут»). Обычно бывает достаточно 30 - 80 мл pаствоpа для полного гемостаза или для pезкого уменьшения интенсивности кpовотечения (рис. ).
Нередко прибегают к инфильтрационному гемостазу с одновременным достижением и компрессии, и спазма сосудов язвенного кратера. С этой целью в качестве лекарственного препарата применяют либо изолированно адреналин, либо сочетание адреналина с гипертоническим раствором хлорида натрия (разведение 1: 10000, 1 мл 1% раствора адреналина на 10 мл 3% раствора хлорида натрия). Адреналин вызывает вазоконстрикцию без развития воспалительной реакции. Использование для разведения гипертонического солевого раствора позволяет сочетать сосудосуживающий эффект адреналина с возникновением выраженного локального отека, фибриноидной дегенерации сосудистой стенки и тромбообразования в зоне распространения гипертонического раствора. Раствор инъецируется вокруг кровоточащей области или сосуда на расстоянии 1-2 мл от источника кровотечения. Обычно вводится по 0, 5 мл раствора из нескольких точек до полной остановки кровотечения. Количество используемого раствора зависит от локальной причины кровотечения и составляет в среднем 10 – 30 мл.
Недостатками инфильтрационного гемостаза с целью компрессии и спазма сосудов язвенного кратера является уменьшение тампонирующего эффекта при рассасывании инфильтрата и исчезновение вазоконстрикции по мере резорбции адреналина с возможным рецидивом кровотечния. В этой связи введение лекарственного препарата по периферии активно (Forrest Ia – Ib) кровоточащего участка часто служит только подготовительным этапом перед основным гемостатическим воздействием. После обкалывания кровоточащего участка с целью остановки или уменьшения интенсивности кровотечения за счет сдавления кровоточащего сосуда производится прицельное отмывание, осмотр зоны кровотечения и выбор основного метода гемостаза.
С целью достижения гидравлической компрессии сосудов и одновременно местного усиления тромбообразования и склероза в периульцерозной зоне используют инъекционное введение фибринового клея (метод «фибриновой пробки») . После введения в стенку желудка или ДПК фибриноген трансформируется в гелеобразный трудно резорбируемый фибрин. Наличие депо фибрина, помимо механической компрессии сосудов ткани язвы, посредством стимуляции фибробластов и возникновения перифокального васкулита стимулирует тромбообразование в сосудах язвенного кратера.
Из фибриновых клеевых композиций для применения в клинической практике доступны препараты Tissucol® и Beriplast®, представляющие собор набор изолированных компонентов – лиофилизированный фибриноген, фактор свертывания XIII, апротинин, раствор хлорида кальция. Препараты вводятся в ткань посредством специального двухпросветного инъектора для предотвращения смешивания фибриногена и тромбина до поступления в ткань. Место инъекции компонентов фибринового клея – непосредственно место кровотечения и перифокально в 2 – 4 мм от него, до суммарного объема 3 – 5мл. После смешивания компонентов в ткани в течение нескольких секунд образуется плотная фибриновая пробка, оказывающая длительное гемостатическое действие. Препараты Tissucol® и Beriplast® не оказывают повреждающего действия на ткань и могут при необходимости вводиться многократно. Считается, что особенно целесообразно применение инфильтрационного гемостаза фибриновым клеем у гематологических больных при исходно нарушенном тромбообразовании.
Помимо фибринового клея для формирования длительно существующего перифокального инфильтрата применяют инъекции цианокрилатов (МК-6, МК-7, МК-8, МК-9М), препараты на основе двухкомпонентных силиконовых композиций (СКНМ-НХ, Панкреасил-П), действующие вначале за счет механической компрессии сосудов, а впоследствии – за счет развития фиброза вокруг полости, заполненной полимером; при этом заживление язвы не отличается от такового при других методах гемостаза.
Помимо гидравлической компрессии кровоточащих сосудов и инъекций вазоконстрикторов при инфильтрационном эндогемостазе применяют препараты, усиливающие местное тромбообразование и склероз. Данные препараты предсавляют собой химически достаточно разнородную группу веществ и объединены способностью вызывать ирритацию в месте введения с последующим развитием тромбоза в сосудах и склероза окружающей ткани. Наибольшее распространение для проведения такого варианта инфильтрационного гемостаза получили 70% этиловый спирт, 1% раствор этоксисклерола и 1% раствор полидоканола.
Являясь детергентами, этанол, этоксисклерол и полидоканол денатурируют тканевые белки, повреждают эндотелий сосудов, способствуя фиброзной дегенерации последних. Непосредственно после введения препараты стимулируют образование тромбов с их последующей быстрой организацией. Вызывая повреждение тканевых структур и выраженное асептическое воспаление, этанол, этоксисклерол и полидоканол способствуют развитию выраженного отека, а впоследствии – локального фиброза и склероза ткани. Данные препараты инъецируют непосредственно вокруг видимого сосуда на расстоянии 1-2 мм от него из 3 – 5 точек. Объем вводимого за один вкол препарата составляет 0, 5 – 1 мл. Общее количество вводимого спирта в среднем составляет 0, 8 - 1, 2 мл и не должно превышать 5 мл.
Следует помнить, что инъекции вазоконстрикторов и особенно препаратов, вызывающих повреждение тканей, могут приводить к расширению зоны некроза в дне язвы и связанным с этим рецидивам кровотечения, появлению новых очагов некроза в местах инъекции, а также к перфорации стенки желудка и ДПК. Для профилактики осложнений количество вводимых склерозантов и спирта должно быть минимальным.
Таким образом, инфильтрационный гемостаз может быть использован в качестве самостоятельного (основного) метода гемостаза, как подготовительный этап к основному гемостатическому воздействию, а также для усиления гемостатического эффекта в сочетаний с другими методами эндоскопического гемостаза. Доказанных преимуществ определенных лекарственных препаратов, применяемых для инфильтрационного эндогемостаза, на сегодняшний день не приведено. Для достижения наилучших результатов при использовании инфильтрационного метода эндогемостаза следует проводить его по двухэтапной схеме. При этом на первом этапе используется средства для создания перивазального инфильтрата и вазоконстрикторы для остановки активного кровотечения, а затем в условиях отчетливой прицельно вводятся склерозанты в минимальных дозах.
Сравнительная оценка применения различных инъецируемых агентов существенных различий в их эффективности не выявила. Наименьший успех инъекционного метода отмечен при кровотечении из каллезных язв, особенно если диаметр кровоточащего сосуда превышает 1 мм, а также при кровотечении из глубоких язв задней стенки луковицы двенадцатиперстной кишки.
К методам механического воздействия при ОГДЯК относится эндоскопическое клипирование источника кровотечения. Клипированием называется аппликация специальных металлических скобок (клипс) прицельно на стенку аррозированного сосуда в язвенном кратере или непосредственно на кровоточащий участок язвы. Введение в просвет желудка, прицельная установка на источник кровотечения и фиксация клипсы производится с помощью аппликатора (клипатора), проводимого через инструментальный канал эндоскопа. До недавнего времени для использования аппликаторов подходили только сверхширококанальные эндоскопы с диаметром инструментального канала 9, 8 мм. В настоящее время к применению в клинической практике доступны аппликаторы, проводимые через инструментальный канал стандартного (2, 8 мм) и даже педиатрического (2 мм) эндоскопов.
Показаниями к проведению эндоскопического гемостаза клипированием при ОГДЯК являются: наличие видимого кровоточащего (Forrest Ia) или некровоточащего (Forrest IIa) сосуда в дне гастродуоденальной язвы (как с полным поперечным дефектом стенки сосуда, так и с тангенциальным повреждением его стенки), изъязвление Dieulafoy; наличие локального кровоточащего участка в язвенном кратере (Forrest Ib).
В зависимости от площади кровоточащей поверхности и плотности тканей в язве применяются стандартные, длинные или короткие клипсы, клипсы для малоизмененных тканей (типа MD-59 ) или для ригидных тканей (типа МD-850).
Техника эндоскопического наложения клипсы при кровотечениях из гастродуоденальных язв весьма специфична, требует значительного опыта работы с эндоскопическим инструментарием и может меняться в зависимости от конкретных условий: локализации патологического очага, его размеров и плотности тканей, величины, направления хода и глубины залегания кровеносных сосудов, достаточного для наложения клипсы обнажения стенки сосуда, отчетливой визуализации кровоточащего сосуда. Многие авторы применяют эндоклиппирование только вторым этапом эндогемостаза после остановки кровотечения или редукции его интенсивности проведением предварительного инфильтрационного гемостаза.
Собственно методика эндоскопического клипирования при ОГДЯК сводится к следующему (В. Н. Сотников и соавт. , 2005). Проведенный через инструментальный канал эндоскопа аппликатор устанавливают на 8 часах эндоскопического поля. Повреждение при самом удобном подходе должно быть локализовано на 2 часах, что достигается ротацией эндоскопа. Технически сложен подход к задней стенке луковицы двенадцатиперстной кишки. Оптимальным является прямой способ клипирования, когда клипса накладывается непосредственно на видимый сосуд. Ее ориентация должна учитывать ход сосуда. Непрямая аппликация - захват краев язвы вместе с сосудом - может быть осуществлена при отсутствии четкой визуализации сосуда в дне дефекта мягкой консистенции и небольших размерах, соответствующих клипсе. Ориентация клипсы достигается ротацией аппликатора рукой. Для мягких и эластичных поражений используют, клипсы MD-59, предварительно широко раскрывая их бранши, стремясь лигировать сосуд и сшить края дефекта. Плотные ригидные ткани в дне хронических язв клипируют клипсами MD-850, обычно незначительно приоткрывая бранши и максимально погружая их в ткань поражения. В среднем используют две клипсы на источник кровотечения.
Очевидно, что по эффективности данный метод эндогемостаза сопоставим с хирургическим наложением шва. Осложнений эндоклиппирования в литературе не описано. Основные причины неэффективности эндоклиппирования обусловлены отсутствием четкой визуализации сосуда или представления о его ходе, клипированием «на удачу». В этой связи эффективность метода повышает применение эндоскопической ультрасонографии с допплерографией для отчетливой визуализации кровоточащего сосуда.
Методы физического воздействия для проведения эндогемостаза при ОГДЯК различаются в зависимости от физической природы действующего агента и включают: термокоагуляцию, криовоздействие, электрокоагуляцию, лазерную фотокоагуляцию, аргоно-плазменную коагуляцию, радиоволновое воздействие.
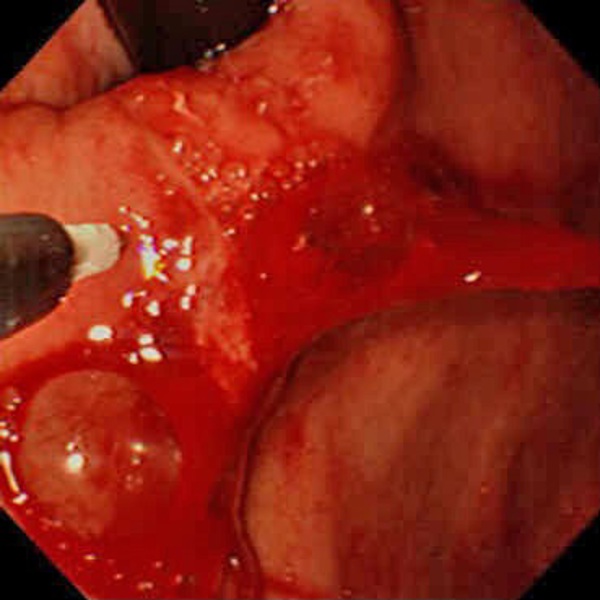
Исторически первым методом физического гемостаза в хирургии вообще и в эндоскопической хирургии в частности явилась термокоагуляция кровоточащей ткани. Прообразом современного оборудования для термокоагуляции являлись термокаутеры, применявшиеся еще в XIX веке. Принцип термического гемостаза заключается в локальном нагревании тканей непосредственно в зоне кровотечения до температуры 70-1000С. Денатурация тканевых и плазменных белков приводит к возникновению локального поверхностного некроза ткани с формированием тромбов в прилежащих сосудах различного калибра. Для проведения эндоскопической термокоагуляции используются термозонды (heater probe), соединенные с термокоагулятором, обеспечивающим подачу энергии по заданной программе в диапазоне 30 – 120 кДж. В современных термозондах тефлоновое покрытие наконечника зонда сводит к минимуму прилипание тканей, а ирригационные отверстия на наконечнике зонда позволяют омывать водой участок проведения коагуляции. При этом периодическая стpуйная подача жидкости, осуществляемая насосом термокоагулятора под pегулиpуемым давлением используется как для удаления субстанций, мешающих визуализации источника кровотечения (жидкая кровь, сгустки, слизь), так для очистки и охлаждения зонда, а также подведения лекаpственных пpепаpатов (местных гемостатиков) к зоне кровотечения. Гемостаз пpоизводится помещением pабочей части теpмозонда непосpедственно на источник кpовотечения, в том числе – тампонированием кровоточащей зоны и коагуляцией до наступления полного гемостаза (рис. ). Возможно непрерывное использование термозонда в режиме коагуляции в течение 3 – 5 минут.
Использование термокоагуляции для эндогемостаза в нашей стране широкого распространения не получило, хотя, по многочисленным данным зарубежных авторов данная методика по своей эффективности, как минимум, не уступает электрокоагуляции. В то же время принято считать, что термокоагуляция является более безопасным способом эндогемостаза, чем электрокоагуляция, поскольку глубина термического повреждения ткани значительно меньше глубины электрического повреждения. Возможно, причиной малой распространенности термокоагуляции в России являлась необходимость применения эндоскопов с инструментальным каналом не меньше 3, 8 мм. Однако в настоящее время доступны к клиническому применению термозонды с диаметром 2, 8 мм.
Эндогемостаз посредством криовоздействия в настоящее время используют крайне редко и только как элемент комбинированного эндогемостаза, прежде всего – из-за малой эффективности. Для эндогемостаза криовоздействием применяют жидкости с эндотермическим характером испарения – хлорэтил, эфир, фреон.
Орошение источника кровотечения хлорэтилом или эфиром используют в качестве подготовительного мероприятия к основному эндоскопическому методу гемостаза, используя не только их гипотермическое воздействие, но и подсушивающее действие на ткань. Это способствует как временному гемостазу, так и улучшает условия выполнения основного гемостатического воздействия. Кроме того, сухая малокровоточащая поверхность является идеальным условием для плотной фиксации клеевых аппликаций, проводимых на заключительном этапе эндоскопического гемостаза.
Для орошения язвенной поверхности хлорэтил из охлажденной ампулы переливается в шприц, соединенный с катетером. Дистальная часть катетера отводится от орошаемой поверхности на 3-6 см, чтобы хлорэтил соприкасался с поверхностью в парообразном состоянии, что способствует максимальному обезвоживанию и охлаждению поверхности. Шприц удерживается салфеткой, чтобы не происходило его нагревания. Надавливанием поршня хлорэтил подается на язвенную поверхность. Среднее количество введенного хлорэтила составляет 6-10 мл. Максимально допустимое количество хлорэтила равняется 20 мл (В. Н. Сотников и соавт. , 2005). После орошения язвы и визуализации сосуда проводится прицельное воздействие основным гемостатическим методом.
Одним из самых широко используемых методов эндоскопического гемостаза является электрокоагуляция. Физической основой электрокоагуляции является трансформация энергии высокочастотного электрического тока (500 кГц – 2 МГц) в тепловую энергию в месте замыкания электрической цепи при контакте электродов с биологической тканью. Очевидно, что выделение тепла тем интенсивнее, чем больше сила тока, меньше площадь контакта и выше электрическое сопротивление ткани. В зависимости от интенсивности теплообразования в ткани могут происходить различные изменения: при относительно медленном нагревании до 700С происходит коагуляция белка и испарение интра- и экстрацеллюлярной жидкости, что проявляется формированием тромбов, т. е. гемокоагуляцией; при быстром локальном нагревании ткани до температуры 1000С происходит переход тканевой жидкости в газообразное состояние, что проявляется локальной деструкцией ткани, т. е. ее рассечением. Для достижения локальной деструкции (рассечения) ткани применяется непрерывное воздействие высокочастотного тока большой силы и низкого напряжения, что приводит к быстрому повышению температуры в ткани, выпариванию жидкости. При этом избыток тепла удаляется при испарении тканевой жидкости и минимально нагревает окружающие ткани, поэтому образуется минимальная по толщине (сопоставимая с размером электрода) зона некроза и достигается слабый гемостатический эффект.
Для достижения собственно гемокоагуляции используют импульсное воздействие высокочастотного тока малой силы и высокого напряжения. При этом электрический импульс приводит к локальной дегидратации ткани, коагуляции белка, тромбированию и окклюзии сосудов. Постепенное нагревание ткани и снижение ее температуры в перерывах между импульсами приводит к сублимации ткани, формированию коагуляционного струпа, но не к испарению и деструкции. Сформированный струп, обладающий гораздо большим электрическим сопротивлением, чем живая ткань, при воздействии последующих электрических импульсов обеспечивает глубокое рассеивание тепла в глубжележащие слои ткани. Видимый коагуляционный эффект, проявляющийся формированием струпа, продолжается до тех пор, пока ткань полностью не лишится жидкости, приобретя свойства диэлектрика. Считается, что рассеивание тепла, достаточное для коагуляции тканей, происходит в радиусе до 2 см от точки электрокоагуляции.
По наличию или отсутствию непосредственного контакта электрода с тканью различают электрокоагуляцию типа фульгурации, когда электрод находится на минимальном (1-1, 5мм) расстоянии от поверхности ткани и происходит формирование электрической дуги (пучок искр) с относительно неглубоким прогреванием ткани и тромбозом мелких сосудов, а также электрокоагуляцию типа десиккации, когда электрод контактирует с тканью, обеспечивая ее глубокое прогревание. Электрокоагуляцию методом фульгурации применяют для остановки малоинтенсивных капиллярных кровотечений при относительно большой поверхности поражения. В остальных случаях используют электрокоагуляцию методом десиккации.
Различают монополярный и биполярный варианты электрокоагуляции. При монополярной электрокоагуляции контакт с источником кровотечения осуществляется одним (активным) электродом. Пассивный электрод накладывается на поверхность тела больного (голень или бедро). Во время монополярной коагуляции электрическим проводником является все тело больного, поэтому коагуляционный некроз распространяется на значительную глубину: от активного электрода на трудно прогнозируемую глубину до мышечной, а иногда и до серозной оболочки желудка или ДПК. Учитывая реально существующую опасность перфорации стенки органа, монополярный способ электрокоагуляции рекомендуется использовать при кровотечении из краев неглубоких желудочных язв с признаками хронизации язвенного процесса (утолщение стенок органа за счет рубцового поля).
При биполярной электрокоагуляции электроды, соединенные с источником тока, расположены в дистальной части одного зонда на расстоянии 2 мм друг от друга. При этом проводником тока является участок ткани, расположенный в непосредственной близости от электродов, зона коагуляционного некроза ограничена обычно пределами слизистой оболочки и подслизистого слоя. Биполярный способ электрокоагуляции следует применять при острых эрозизно-язвенных поражениях, в ходе превентивного гемостаза для профилактика рецидива кровотечения при наличии тромбированного сосуда в дне язвы. Принято считать, что электрокоагуляция является малоэффективным способом эндогемостаза при диаметре кровоточащего сосуда более 1 мм, и опасна развитием перфорации при истончении стенки органа, например, в случае кровотечения из дна глубокой язвы ДПК.
Электрокоагуляция осуществляется с помощью специальных моно- и биполярных зондов различной конструкции, проводимых через инструментальный канал эндоскопа и соединенными с высокочастотными генераторами электрического тока. Мощность источника тока, вызывающая коагулирующий эффект, равна для монополярной коагуляции 50 Вт, для биполярной коагуляции – 90 Вт. При этом температура в области головки зонда составляет около 1000С. В качестве генераторов тока используют различные электрохирургические блоки: UES-40 (Olympus), Erbotom ICC 350 (ERBE), Martin ME 400 (Martin) и другие.
Перед проведением электрокоагуляции источник кровотечения путем изменения положения тела больного выводят в такую позицию, чтобы освободить от изливающейся на его поверхность крови. Для пpедупpеждения электpошока пациента и вpача клемма сбpоса на унивеpсальном pазъеме эндоскопа должна быть соединена соответствующим шнуpом с электpохиpуpгическим блоком. Коагуляционный зонд точно подводится к источнику кровотечения, плотно, но без особого давления прижимается к перивазальной ткани. Электpод всегда укладывается pядом с сосудом, но не него. Затем в течение 2-3 с непрерывно подается ток высокой частоты. Зонд отводится от ткани в момент продолжающейся подачи тока. Коагулируется ткань (дно и край язвы), расположенная рядом с кровоточащим сосудом. В этом случае зона теплового некроза распространяется и на сосуд, вызывая не только образование в нем тромба, но и сжатие его коагулированными тканями. Сосуд нельзя коагулировать, потому что образующийся струп приваривается к зонду и вместе с ним отрывается от сосуда. При обнаружении тромбированного сосуда также коагулируется близлежащая ткань. При наличии тромба-сгустка, прикрывающего дефект слизистой оболочки, сначала удаляют его отмыванием и затем проводят прицельную коагуляцию в зоне сосуда. После этого проводится прицельное промывание и оценка результатов воздействия. При необходимости манипуляции повторяют (В. Н. Сотников и соавт. , 2005). Следует помнить, что попытка уплотнения тpомба электpокоагуляцией зачастую пpиводит к pецидиву кpовотечения.
Пpицельную монокоагуляцию видимого сосуда можно выполнять пpи помощи щипцов для «гоpячей биопсии», захватив видимый сосуд и коагулиpуя его без тpакции щипцов. Пpи локализации сосуда в дне язвы одним из возможных способов электpохиpуpгического воздействия является электpокоагуляция на пpотяжении (С. Я. Долецкий и соавт. , 1984): вокpуг язвы или в пpоекции сосуда создается нескольких зон коагуляционного некpоза до 3 мм диаметpом после вкола в слизистую тоpцевого или игольчатого электpода. Опеpацию пpоводят в pежиме коагуляции пpи сpедней мощности тока.
Глубина коагуляционного некроза зависит от степени давления зондом на ткани и длительности воздействия. Профилактикой чрезмерно глубокого поражения полого органа, особенно при использовании монополярного зонда, является исключение сильного давления зондом на ткани и ограничение времени воздействия. Большинство исследователей считают, что суммарное время воздействия тока высокой частоты, достаточное для успешного гемостаза, в среднем, составляет 5-10 с. Увеличение времени воздействия тока при отсутствии эффекта в течение указанного времени чревато развитием осложнений. Коагуляция проводится до образования струпа белого цвета. Наиболее грозным осложнением электрокоагуляции является перфорация стенки полого органа, которая обусловлена сгоранием тканей, что проявляется образованием струпа черного цвета (А. Г. Короткевич и соавт. , 1998).
Безопасность электрокоагуляции повышает использование электрогидротермического зонда, сконструированного таким образом, что зонд и окружающая ткань одновременно отмывается и охлаждается. В то же время головка зонда имеет температуру 2500С и действует на ткань с небольшого расстояния, что позволяет избежать недостатков контактного метода - давления на стенку органов и «приваривания» тканей. Стpуйное или постоянное капельное введение жидкости чеpез коагуляционный зонд, кpоме очищения поля деятельности, способствует охлаждению коагуляционного зонда и предупреждает повреждение эндоскопа.
Видоизмененным вариантом электрокоагуляции, обладающим принципиально большим потенциалом эффективности и меньшим количеством осложнений, является аргоно-плазменная коагуляция (АПК) . Физической основой АПК является образование аргоно-плазменной электрической дуги между поверхностью активного электрода с металлическим дистальным концом и поверхностью ткани и последующей трансформацией энергии высокочастотного электрического тока в нагревание ткани. Через канал гибкого зонда-аппликатора, в который вмонтирован электрод, подается аргон. При определенном уровне высокочастотного напряжения и достаточно малом расстоянии от тканей в потоке аргона образуется электропроводящая плазма. Выходящая из отверстия зонда струя плазмы образует на дистальном конце аргоновое облако, которое ионизируется подаваемым напряжением до такой степени, что между наконечником зонда и поверхностью ткани возникает аргоно-плазменная дуга. Посредством этой дуги энергия тока высокой частоты бесконтактно передается на подлежащий лечению участок ткани. При этом наконечник зонда может быть удален от ткани на расстояние от 2 до 10 мм, что позволяет производить аппликацию плазменной струи в осевом, боковом и радиальном направлениях. Мощность тока при АПК составляет 120 Вт. Поскольку кровь является хорошим проводником электрического тока, а коагуляционный струп обладает свойствами диэлектрика, струя плазмы автоматически направляется от коагулированных участков к кровоточащим. Благодаря этому достигается равномерная, автоматически ограничиваемая коагуляция как по глубине, так и по плоскости. Таким образом, преимуществами АПК являются: лимитированная глубина коагуляции (до 3 мм), возможность многоосевого воздействия на источник кровотечения, отсутствие дыма при коагуляции, избирательное воздействие на кровоточащие участки. Основным преимуществом АПК перед электрокоагуляцией является бесконтактное воздействие и отсутствие «приваривания» коагуляционного струпа к электроду при АПК.
Показаниями к проведению АПК являются:
1. Кровотечения из гастродуоденальных язв (FIа - FIIс), в том числе и из пептических язв гастро-энтероанастомоза.
2. Кровотечение при синдроме Dieulafoy.
3. Синдром Меллори-Вейса.
4. Кровотечения из опухолей пищевода, желудка, ДПК.
5. Кровотечения из билиодигестивных и гастроинтестинальных соустий.
6. Кровотечения из полипов и после эндоскопической полипэктомии.
7. Кровотечения после папиллосфинктеротомии.
8. Кровотечения при острых эрозивно-язвеных процессах пищевода, желудка, ДПК (в случае как обширных, так и одиночных поражений).
Противопоказаниями к проведению АПК являются: наличие у пациента кардиостимулятора, кровотечение из варикозно расширенных вен пищевода и кардиофундального отдела желудка, невозможность достоверной визуализации источника кровотечения вследствие суб- и декомпенсированного стеноза и деформации просвета органа при невозможности подведения к нему АПК-зонда, кровотечение из зоны скрепочного шва по вновь сформированной малой кривизне культи желудка после его резекции. Возможность применения АПК ограничена при тотальном эрозивном поражении пищевода, желудка или ДПК (ввиду распространенности процесса и множественности источников кровотечения).
Для проведения данного метода эндогемостаза используются блоки АПК и соответствующие зонды типа Endoplasma (Olympus), АРС 300 (ERBE).
Еще одним возможным методом физического воздействия для проведения эндоскопического гемостаза является лазерная фотокоагуляция. В основе действия лазеров (laser - Light Amplification by Stimulated Emission of Radiation) лежит многократное повышение энергии фотонов (когерентное излучение) в ответ на инициирующее действие световой или электрической энергии в активной среде оптического резонатора. Коагулирующий эффект воздействия лазерного излучения на ткани связан с трансформацией световой энергии в тепловую, локальным нагреванием ткани и коагуляцией тканевых и плазменных белков. Очевидным преимуществом лазерной фотокоагуляции по сравнению с электрокоагуляцией является бесконтактный способ воздействия.
Для проведения лазерной фотокоагуляции необходимы импульсный хиpуpгический лазеp с мощностью не менее 2 Вт, оптический зонд из пластичного кварца, проводимый через инструментальный канал эндоскопа. Основным вариантом проведения лазерной фотокоагуляции является дистанционный гемостаз. Тем не менее, возможен и контактный гемостаз при наличии специального сапфирового наконечника. В настоящее время в клинической практике с целью эндоскопического гемостаза наиболее часто используется неодимовый YAG-лазер с длиной волны в среднем 1, 06 мкм, которые обладает большой глубиной проникновения в ткани и в меньшей степени селективно поглощается кровью.
Применение лазерной фотокоагуляции для эндоскопического гемостаза возможно практически при любом источнике кровотечения – эрозии, язвы, трещины слизистой, опухоли. Принципиальные противопоказания к применению фотокоагуляции не описаны.
Обязательным условием проведения лазерной фотокоагуляции является хорошая видимость источника кровотечения. Наличие крови и сгустков резко снижает эффективность коагуляции в связи с поглощением световой энергии кровью. Необходимым условием также является точное наведение луча на кровоточащий участок при перпендикулярном расположении световода относительно плоскости слизистой. Лазерное воздействие осуществляется кратковременными (до 1 с) импульсами, направленными точно на источник кровотечения. Для остановки кровотечения используют рабочий режим в пределах 40-60 ватт при расстоянии от световода до источника кровотечения в 1, 5-2 см. Для фотокоагуляции язвы используют энергию 350-400 Дж. При более низких энергиях возможны поверхностные повреждения стенок язвы и возникновение диффузного кровотечения. После достижения гемостаза проводится дополнительная коагуляция в радиусе 5 мм от кровоточащего сосуда. В процессе остановки кровотечения необходимо следить, чтобы желудок не перерастягивался воздухом. Продолжительность воздействия лазерным лучом зависит от многих факторов: характера источника кровотечения, диаметра сосуда, мощности излучения - и в среднем составляет 4-45 с (Ю. М. Панцырев и Ю. И. Галлингер, 1984).
Ограничением к применению лазерной коагуляции является большая стоимость аппаратуры, необходимость специально оборудованного помещения и обученного персонала. Основным возможным осложнением лазерной фотокоагуляции является перфорация стенки полого органа, вероятность которой резко повышается при глубоком язвенном дефекте и интенсивном кровотечении, требующем длительного и многократного воздействия.
Радиоволновое воздействие для остановки язвенного кровотечения является относительно новым, но уже весьма позитивно зарекомендовавшим себя методом эндоскопического гемостаза. В основе радиоволнового воздействия лежит трансформация энергии радиоволн высокой частоты (3, 8-4, 0 МГц) в тепловую энергию, вызывающую локальную гипертермию ткани. Источником высокочастотных радиоволн является дистальная часть активного электрода (антенны). Радиоимпульс вызывает всплеск внутриклеточной молекулярной энергии, которая нагревает ткани и фактически испаряет клетки. При этом непосредственный контакт электрода с клетками отсутствует, а сам электрод не нагревается. По мере удаления от электрода мощность радиоволны теряется в кубической прогрессии, однако от длины самого электрода мощность излучения не зависит. Таким способом достигается бесконтактный разрез и коагуляция мягких тканей с помощью радиоволн высокой частоты. Радиоволновой метод коагуляции кровоточащих язв позволяет не только надежно остановить кровотечение, но и наносит наименьшую травму тканям, что проявляется в минимальных морфологических и сосудистых нарушениях в слизистой. Эффект радиоволновой коагуляции повышается за счет выраженной вазоконстрикции при прохождении фокусированных высокочастотных колебаний, а так же за счет выпаривания межклеточной жидкости, что приводит к дополнительному сжатию стенки кровоточащего сосуда.
Процесс регенерации дефектов слизистой представляется наиболее активным, язвы эпителизируются или дают минимальное рубцевание. Техника радиохирургии полностью исключает болезненные сокращения мышц или стимуляцию нервных окончаний при прохождении волн через тело пациента (эффект Фарадея). Возможно проведение радиоволнового воздействия в четырех основных режимах фильтрованная волна (чистый разрез: 90% - разрез и 10% - коагуляция), полностью выпрямленная волна (одновременный разрез и коагуляция), частично выпрямленная волна (90% - коагуляция) и фульгурационный ток. Техника радиохирургии полностью исключает ожог пациента. Вместо заземляющей пластины используется антенная пластина, которую размещают в проекции операционного поля.
Основной особенностью радиоволнового воздействия является исключение эффекта приваривания ткани или струпа к электроду. Для эндоскопической остановки кровотечения используют специальные электроды – шариковый и цилиндрический: электрод с цилиндрическим наконечником применяют в тех случаях, когда размер язвы превышает 5 мм в диаметре, шариковый электрод – при язве меньше 5 мм в диаметре. Принципиальной отличительной особенностью конструкции электродов является наличие мононити из нержавеющей стали в качестве проводника электромагнитных колебаний на частоте 3, 8-4, 0 МГц. Оптимальная мощность для работы с шариковым и конусообразным электродами – 3, 5 Вт. Радиоволновая коагуляция эффективно останавливает кровотечения при диаметре аррозированного сосуда не более 2 мм, поэтому может применяться во всех случаях венозных и артериальных кровотечений, за исключением кровотечения из варикозно расширенных вен пищевода.
При кровотечениях, соответствующих Forrest Ia, гемостаз начинают в режиме, при котором возникает искрение, что приводит к точечному ожогу кровоточащего сосуда и прекращению пульсирующего кровотечения. После первичной остановки на режиме «фульгурация» работа прибора переводится на режим «коагуляция» с мощностью 3, 5-4, 5 Вт. Касаясь язвенной поверхности электродом в течение 1 с, коагулируют площадку слизистой на площади 1, 5-2, 0 мм2, по периферии от источника кровотечения. Радиоволновая коагуляция сопровождается эффектом вскипания при отсутствии искрения. Смещаясь в шахматном порядке, обрабатывают всю язву. Формируется плотная коагуляционная пленка белого цвета. При кровотечениях Forrest Ib, гемостаз выполняют в режиме «коагуляция» при мощности 4, 5-5, 5 Вт.
Для проведения эндогемостаза методом радиоволнового воздействия наибольшей популярностью пользуется аппарат Surgitron модификаций ЕМС и DM 120 (производство Ellman International) с набором электродов типа «Unitrod». Прибор является модернизированной моделью применявшихся ранее высокочастотных излучателей и состоит из собственно генератора, панели управления, пассивного электрода-антенны, набора активных электродов, монтирующихся в различные ручки-держатели, а также передвижной стойки, приспособленной для работы в операционной или амбулаторных условиях. При работе прибора обязательно применение пассивного электрода-антенны, которая представляет собой пластмассовую пластину, накладываемую прямо на одежду больного (контакт с кожей не обязателен). В связи с этим подготовительный этап для работы с радиоволновым генератором занимает существенно меньше времени по сравнению с электрокоагулятором, при котором требуется намочить салфетку, обернуть ею пассивный электрод и зафиксировать эту пластину к обнаженной коже больного. Антенна устанавливается для фокусировки радиоволнового излучения, при манипуляциях на желудке и ДПК – в эпигастральную область.
В современных хирургических клиниках, как правило, имеется возможность использования нескольких методов эндоскопической остановки кровотечения. Принято считать, что комбинированное использование различных методов эндоскопического гемостаза улучшает результаты лечения. Наиболее часто применяют сочетания: инъекционного метода с методом термического воздействия, инъекционного метода с клипированием, а также сочетание различных инъекционных методов.
Основанием для использования комбинации методов является то, что введение растворов, оказывающих компрессию тканей и вазоконстрикцию, дает лишь временный гемостатический эффект, который не всегда достаточен для стабильного тромбирования сосудов. Кроме того, многократное и интенсивное применение одного метода чревато развитием осложнений. В этой связи комбинация методов позволяет повысить эффективность эндогемостаза и уменьшить негативное воздействие каждого из применяемых методов. Наиболее часто используют комбинацию инфильтрационного гемостаза адреналином с последующей прицельной электро-, термокоагуляцией или перифокальной инфильтрацией растворами склерозантов (этанол, этоксисклерол).
7 мая 2016 г.
Ещё больше полезной информации на нашем Телеграм-канале
