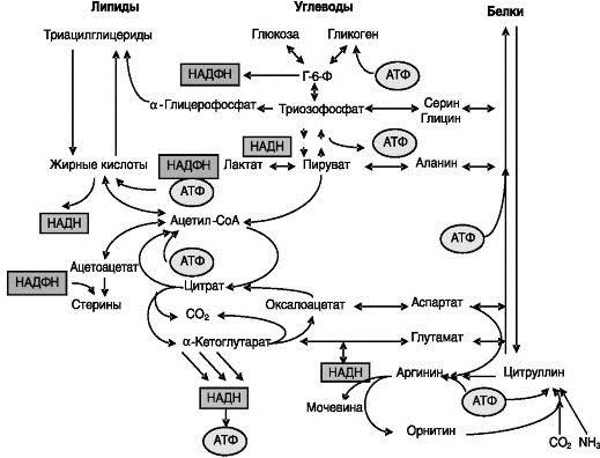
Даже при раздельном рассмотрении обмена углеводов, белков и жиров становится очевидным, что эти виды обмена тесно связаны между собой. Эта связь осуществляется на разных уровнях и проявляется в разных формах. Основой для взаимосвязи служат отношения между белками, углеводами и липидами как субстратами и продуктами взаимопревращений с общим энергообеспечением и общими конечными продуктами обмена (рис. 1. 9. ). При акцентировании внимания на общем энергетическом обеспечении разных видов обмена можно отметить, что в анаболических процессах биосинтеза белков, липидов или углеводов используются одни и те же источники энергии фосфорилирования (АТФ) или восстановления (НАД (Ф) Н), которые пополняются за счет катаболических процессов распада поступающих с пищей или эндогенных белков, липидов или углеводов. При этом между процессами биосинтеза белков, липидов и полисахаридов имеется конкуренция за источники энергии. Обращает на себя внимание, что в реакциях различных типов обмена имеются общие предшественники и промежуточные продукты. Еще Кребс и Корнберг отмечали, что, несмотря на огромное разнообразие пищевых веществ (белки, жиры, углеводы), число химических реакций, обеспечивающих их превращения (распад) и образование энергии, «удивительно мало». Среди многих общих продуктов и субстратов, образующихся и используемых в процессах обмена белков, липидов и углеводов, можно выделить как наиболее значимые образующиеся при гликолизе триозы, которые могут быть использованы для образования глицерина (липосинтез) или ряда аминокислот (синтез белка), а также ацетил-КoA. Этот промежуточный продукт образуется при распаде белков, липидов и углеводов и может быть использован для липосинтеза или для извлечения энергии. Пируват образуется в результате гликолиза, или в ходе превращения липидов, а также из аланина (реакцией переаминирования). Пируват может превращаться в лактат, в аланин, участвуя в синтезе белка, в оксалоацетат, участвуя в глюконеогенезе, в ацетил-КоА, используемом в цикле Кребса. Ацетил-КоА может образовываться из пирувата (а, следовательно, и из аланина или глицерола) и из жирных кислот. Ацетил-КоА поступает в цикл трикарбоновых кислот, а также может использоваться при β-окислении жирных кислот. Очевидно, что в процессе катаболизма все три вида обмена имеют общий конечный путь диссимиляции. Образующийся при распаде белков, липидов и углеводов ацетил-КoA поступает в цикл трикарбоновых кислот (цикл лимонной кислоты, или цикл Кребса), где подвергается окислению до углекислого газа. Образующиеся при этом восстановительные эквиваленты в форме НАД (Ф) Н используются далее в дыхательной цепи для получения АТФ. Углекислый газ может быть использован для синтеза жирных кислот (через малонил-КoA) и мочевины, пуринов и пиримидинов (через карбамоилфосфат), причем в мочевине конечные продукты обмена белков, липидов и углеводов (углекислота и аммиак) связаны между собой непосредственно.
Взаимосвязь различных видов обмена может быть прослежена не только на химическом, но и на тканевом и органном уровнях. Очевидно, что в связи с разделением функций между клетками разных органов и тканей в многоклеточном организме между ними происходит постоянный обмен углеводами, липидами и аминокислотами. При этом, как известно, центральную роль в координации обменных процессов и поддержании гомеостаза занимает печень. Она осуществляет внешнюю и внутреннюю секрецию и получает метаболическую информацию через системный кровоток и от кишечника. Благодаря экспрессии ряда ферментов, характерных преимущественно или исключительно для печени, именно в печени протекает ряд жизненно важных обменных процессов. Печень выполняет функции стабилизатора количества глюкозы и аминокислот в организме, играет важнейшую роль в адаптации обменных процессов к режиму питания, в том числе посредством перераспределения потоков питательных веществ между разными органами и тканями. Питательные вещества из кишечника направляются в печень, где подвергаются первичной переработке. Часть поступающих углеводов запасается в печени в форме гликогена, а избыток в виде глюкозы поступает в общий кровоток, откуда она извлекается жировой тканью для превращения в жиры и запасания. Жирные кислоты триглицеридов пищи в печени частично подвергаются дегидрогенизации и направляются в форме ЛОНП в жировые депо. В условиях голодания гидролиз гликогена печени обеспечивает поддержание константы гликемии, а энерогозатраты большинства органов покрываются кетоновыми телами, которые образуются в печени из жирных кислот, поступающих из жировой ткани в результате липолиза. В условиях покоя энергетические затраты скелетной мышцы покрываются преимущественно за счет аэробного процесса окисления жирных кислот. При интенсивной работе в мышце начинает преобладать анаэробный процесс гликолиза. Образующийся в результате лактат поступает в печень, где вновь превращается посредством глюконеогенеза в глюкозу, которая направляется в мышцу. В условиях голодания аминокислоты белков мышцы становятся субстратом для глюконеогенеза в печени, что способствует поддержанию эугликемии, а основным энергетическим субстратом для мышцы становятся кетоновые тела, образующиеся в печени из жирных кислот. Мозг является важнейшим потребителем глюкозы, и эугликемия, поддерживаемая печенью, служит одним из факторов его нормальной работы. Образующийся в процессе жизнедеятельности мозга аммиак (в частности, из нейромедиаторных аминокислот) является нейротоксичным и должен эффективно удаляться из мозга. Это удаление происходит путем связывания аммиака в глутамате и глутамине и их транспортировки в печень, где аммиак высвобождается и превращается в преобладающий конечный продукт азотистого обмена - мочевину. Остающийся после дезаминирования α-кетоглутарат превращается в печени в глюкозу, что способствует эугликемии. В условиях ацидоза, вызванного, например, интенсивной работой, голоданием или диабетом, главным способом выведения избытка протонов из организма становится их связывание с аммиаком и экскреция почками в виде иона аммония. Источником аммиака служит глутамин, поставляемый печенью. Образующийся в почках после дезаминирования глутамина α-кетоглутарат используется для синтеза глюкозы. В условиях голодания это способствует поддержанию эугликемии, а при диабете усугубляет гипергликемию. Таким образом, углеводный, белковый и жировой обмен, составляющих общую цель метаболизма, объединены общими механизмами регуляции: наличием общих лимитирующих реакций и ферментов; аллостерическим характером регуляции ключевых ферментов; наличием общих метаболитов; возможностью быстрого переключения с одного метаболического пути на другой, за счет наличия общих метаболитов, а также принципиально одинаковым механизмом гормональной регуляции.
Взаимосвязь различных видов обмена определяется также общими принципами нейро-гуморальной регуляции с оценкой ее эффективности. При этом имеющиеся в данный момент направленность и интенсивность обменных процессов зависят не только от доступности субстратов и энергии, но и от активности ферментов, катализирующих превращения веществ, и от активности транспортных систем. Регуляции активности ферментов является многоуровневым процессом. Коррекция интенсивности и направленности обменных процессов проводится как на уровне ферментов-исполнителей, так и надстроечными системами регуляции. Обратная связь с контролирующими метаболизм системами осуществляется структурами, воспринимающие уровень метаболитов, сенсорами или рецепторами. Практически во всех клетках организма имеются сенсоры углеводов и липидов, а также уровня энергообеспеченности клетки. Примерами клеток, реагирующими на такие сигналы изменением продукции гормонов служат α- и β-клетки поджелудочной железы (глюкагон и инсулин соответственно), а также адипоциты (лептин, адипонектин, резистин). Сигналы, поступающие в ЦНС извне и в форме изменений в концентрации глюкозы, аминокислот, гормонов желудочно-кишечного тракта, преобразуются в изменения активности симпатико-адреналовой и гипоталамо-гипофизарной систем, что сопровождается модуляцией уровня периферических гормонов, регулирующих активность разнообразных ферментов метаболизма.
По общей направленности действия гормоны условно делят на две большие группы - анаболические и катаболические. Анаболические гормоны способствуют процессам роста и запасания, интегральным показателем которых служит положительный азотистый баланс (преобладание задержки азота в организме над его выведением). Катаболические гормоны действуют противоположным образом.
Катаболические гормоны | Анаболические гормоны |
Катехоламины | Соматотропный (исключение - липолиз) |
Глюкагон | Инсулин |
Кортизол | Тироксин (исключение - липолиз) |
Глюкокортикоиды (исключение - анаболизм в печени) | Андрогены. эстрогены |
Необходимо отметить, что мишени действия разных гормонов одной группы могут совпадать лишь частично, и один и тот же гормон может действовать противоположным образом на клетки разных тканей. Так, например, инсулин влияет на углеводный обмен, активируя транспорт глюкозы через клеточную мембрану, ускоряя окислительный распад глюкозы (активирует ферменты цикла Кребса) ; ускоряет гликогеногенез в печени и мышцах, тормозит гликогенолиз и глюконеогенез. Одновременно с этим инсулин принимает участие в регуляции жирового обмена, ускоряя липогенез из продуктов распада сахаров и замедляя липолиз. Кроме того инсулин ускоряет протеиногенез из продуктов распада сахаров. все эти процессы в конечном счете приводят к снижению концентрации глюкозы в плазме крови. В противоположность этому глюкагон ускоряет распад гликогена и глюконеогенез в печени, ограничивает активность гликогенсинтетазы под действием инсулина. Кроме того глюкагон тормозит синтез белка, ускоряет протеолиз, уменьшает использование глюкозы в процессе синтеза аминокислот, результатом чего является повышение уровня глюкозы в плазме крови. Помимо указанных в регуляции обменных процессов принимают участие многие другие сигнальные соединения. Например, ФНО-α служит важнейшим индуктором кахексии (истощения) при воспалительных заболеваниях, индуцируя, в частности, липолиз. При беременности к регуляции обменных процессов подключаются гормоны плаценты, обеспечивающие мобилизацию материнских запасов и направление их к растущему плоду. Индуцированное стрессорными факторами поступление вазопрессина в передний гипофиз меняет направленность действия этого гормона на катаболическую (через стимуляцию секреции АКТГ и глюкокортикоидов) (по В. А. Ткачуку и А. Н. Смирнову, 2009).
Таким образом, скорость распада одних питательных веществ и биосинтеза других во взаимосвязанных процессах катаболизма и анаболизма, контролируемая многоуровневой регуляторной системой, определяется прежде всего физиологическим состоянием и потребностями организма в энергии и метаболитах. Благодаря динамичности и координации метаболической активности обеспечивается постоянство структуры и функции организма. В нормальных условиях существования метаболизма в широком смысле является саморегулируемым и вполне самодостаточным. Нарушения этого динамического статуса организма, не способные к самостоятельной коррекции, сопровождаются развитием патологических процессов, тяжесть и продолжительность которой будут определяться степенью повреждения структуры и функций отдельных молекулярных и надмолекулярных компонентов клеток.
31 мая 2016 г.
Ещё больше полезной информации на нашем Телеграм-канале