Основными методами диагностики рака предстательной железы на сегодняшний день являются пальцевое ректальное исследование (ПРИ), определение уровня простатспецифического антигена (ПСА), трансректальное ультразвуковое исследование (ТРУЗИ) и выполнение биопсии предстательной железы. Подобный подход к диагностике этого заболевания общепринят как в России, так и в мировой практике.
Методика пальцевого ректального исследования является первичным звеном клинического обследования пациентов с подозрением на рак предстательной железы. Однако эта методика является субъективной, мнение различных специалистов на предмет наличия или отсутствия плотных зон обладает сильной вариабельностью. Пальцевое ректальное исследование имеет чувствительность, специфичность, положительный прогностический тест (ППТ) и отрицательный прогностический тест (ОПТ) 64%, 97%, 47%, 99% соответственно. Следует отметить, что только в 85% случаев рак простаты локализуется в периферической зоне, и может быть выявлен при ПРИ.
В последние десятилетия в мировой практике для скрининга рака простаты стал использоваться анализ сыворотки крови на простатспецифический антиген. ПСА был открыт в 1970 году Ablin et al. ; в 1979 году ПСА был впервые выделен из семенной жидкости исследователем Naga. В том же году Wang et al. установил наличие ПСА в ткани предстательной железы (ПЖ) и обнаружил зависимость между уровнем ПСА и раком предстательной железы. В диагностике РПЖ методика определения ПСА стала широко использоваться лишь с 1987 года.
ПСА - белок, вырабатываемый нормальной предстательной железой. Уровень общего ПСА определяется путем сложения значений свободного ПСА и ПСА, связанного с белками плазмы. Пороговым значением уровня общего ПСА считается 4, 0 нг/мл.
Общеизвестно, что ПСА является органо-специфичным антигеном, но не обладает высокой специфичностью для рака простаты – уровень этого антигена в сыворотке крови может также повышаться в случае доброкачественной гиперплазии предстательной железы и простатита. Фактически, любой воспалительный процесс органов малого таза может вызвать повышение уровня ПСА. На концентрацию ПСА в сыворотке крови может влиять физическое воздействие на простату и выполнение различных манипуляций. Например, массаж ПЖ, ПРИ, термо- и физиотерапия, выполнение ТРУЗИ, биопсия ПЖ; катетеризация, бужирование уретры; эякуляция у пациента накануне взятия биоматериала. Кроме того, уровень ПСА может снижаться под воздействием некоторых лекарственных препаратов: например, при приёме финастерида (проскара), дутастерида, происходит снижение уровня ПСА на 50%.
Процент выявления опухолевых клеток после биопсии у пациентов со значениями ПСА, находящимися в так называемой «серой зоне» (от 3 или 4 нг/мл до 10 нг/мл), по данным Postma R. et al, составляет всего 20-25%. Рак предстательной железы может встречаться и у пациентов с низким уровнем ПСА (менее 4 нг/мл). Наибольшая выявляемость клеток рака предстательной железы отмечается у пациентов с ПСА более 10 нг/мл. В связи с недостаточной чувствительностью и точностью методики определения ПСА, особенно при повышении общего его значения в пределах т. н. «серой зоны», стали использоваться другие, альтернативные модификации антигена.
Плотность ПСА (ПСА - D) – еще одна модификация простатспецифического антигена. Следует отметить, что на значение ПСА во многом оказывает влияние объем ПЖ, учитывая тот факт, что рак ПЖ почти в половине случаев встречается в сочетании с доброкачественной гиперплазией предстательной железы (ДГПЖ). В связи с этим был открыт ПСА - D. Рассчитывается ПСА - D путем деления уровня общего ПСА (в единицах нг/мл) на объем ПЖ (в кубических сантиметрах (куб. см. ) ). По данным работ группы исследователей Akdas A. et al. и Isikay L. et al. , опубликованных еще в 1995-1996 годах, показатель ПСА - D увеличивает специфичность показателя общего ПСА сыворотки крови. Значение индекса ПСА - D не должно превышать 0, 15 нг/мл/куб. см. Объем предстательной железы определяется при ТРУЗИ и вычисляется по формуле эллипса. Однако вычисление объема предстательной железы сильно зависит от методики исследования, а также опыта специалиста. Согласно данным Braeckman et al. , методика определения плотности ПСА обладает низкой воспроизводимостью – расчет объема простаты сильно зависит от исследователя, выполняющего измерения.
Определение скорости прироста ПСА (ПСА V) также широко используется в клинической практике, особенно при необходимости динамического наблюдения за пациентами. Этот тест является высокоспецифичным и основывается на длительном измерении уровня общего ПСА в течение продолжительного срока времени. Наиболее характерным для рака простаты является показатель ПСА V, превышающий или равный 0. 75 нг/мл/год. Ограничениями данного метода являются трудность в подсчетах, зависимость от различных методик подсчета общего ПСА в различных лабораториях, и вариабельная прогностическая ценность, обусловленная возрастом пациента и изначальным уровнем общего ПСА.
Соотношение общего к свободному ПСА (f/t ПСА) по данным ряда авторов является более чувствительным тестом по сравнению с определением общего ПСА, выражается в процентном соотношении. Референсным пределом считается пороговое значение, составляющее 15%. Прогностическая ценность f/t ПСА увеличивается с ростом уровня общего ПСА, и становится наибольшей при его уровне более 6-8 нг/мл. В основном этот тест используется для принятия решения о проведении биопсии у пациентов отсутствием изменений при ПРИ, c уровнем ПСА, колеблющемся в пределах от 4 до 10 нг/мл. По данным проспективного мультицентрического исследования Catalona et al. , было получено 56% подтвержденных биопсий у пациентов с соотношением ниже 10%, и только у 8% пациентов с соотношением более 25%. В то же время, этот тест имеет ошибки при значениях от 10 до 25%, сильно зависит от нестабильности и колебания уровня свободного ПСА, а также наличием у пациента ДГПЖ.
Про-ПСА (также известный как p2ПСА), является специфической изоформой профермента ПСА. Данный биомаркер был предложен к использованию, чтобы увеличить обнаружение рака простаты у мужчин с уровнем общего ПСА, колеблющемся в пределах между 2, 0 до 10, 0 нг/мл. Согласно некоторым проспективным исследованиям, применение анализа р2ПСА позволяет уменьшить количество ненужных биопсий простаты на 7, 6-35%, при этом чувствительность теста достаточно высока и составляет 95%. Клиническая значимость этого биомаркера пока не определена.
ПСА 3 – антиген рака предстательной железы 3 гена (PCA3), который был идентифицирован в 1999 г. По гистологическим данным, этот антиген избыточно экспрессируется почти во всех образцах ткани рака предстательной железы, но не в нормальной или гипертрофированной ткани. Уровень PCA3 определяется путем вычисления соотношения PCA3 мРНК и ПСА мРНК в анализе мочи, собранном после выполнения ПРИ или массажа простаты. Наиболее часто определение уровня PCA3 используется для принятия решения о выполнении биопсии, когда уровень общего ПСА находится в пределах от 2, 5 до 10, 0 нг/мл, а также для мужчин с ранее отрицательными биопсиями в анамнезе, у которых имеется устойчивое повышение уровня общего ПСА.
Использование антигена PCA3 может играть значительную роль в снижении количества необоснованных биопсий, однако в настоящее время нет достаточного количества данных о клинических результатах, подтверждающих возможности его рутинного применения.
Генетическую основу развития РПЖ позволяют исследовать молекулярно-генетические методы, геномные и транскриптомные технологии. К повсеместно используемым технологиям относятся ДНК-микроэррэй, ПЦР, ПЦР в режиме реального времени, флуоресцентная гибридизация in situ. С помощью этих методов можно выявить изменения ДНК, которые могут служить маркерами опухолевого процесса, а также обнаружить потенциальные маркеры путем сравнения уровней продуктов транскрипции тысяч генов в нормальных и раковых тканях. Сегодня зарубежными исследователями активно осуществляются поиск и разработка новых, более эффективных маркеров РПЖ, таких как p2PSA, генотип CYP3A4, Ki67 LI, Bcl-2, p53, syndecan-1, CD10, циркулирующие опухолевые клетки (CTCs), цитокератин, СК 8, СК 18, СК 19, человеческий эпителиальный антиген, молекулы адгезии к эпителиальным клеткам (EpCAM), PSMA, PSA/RTPCR, PSCA, PCA3, ЕРСА, AMACR и др.
Пушкарь Д. Ю. и соавт. считают, что до сих пор не существует единой точки зрения на значения нормы показателей различных методик измерения ПСА, что не позволяет однозначно оценивать клиническую значимость этих методик.
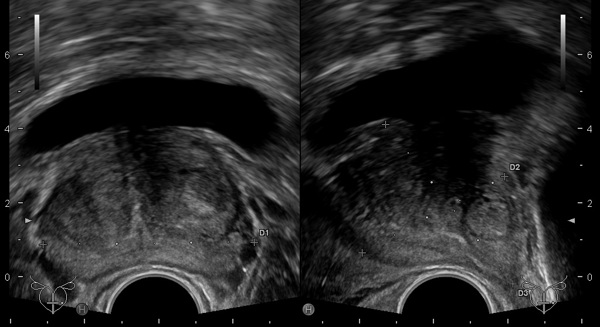
В настоящее время трансректальное ультразвуковое исследование получило широкое распространение как наиболее экономичный, простой и в то же время достоверный скрининговый метод визуализации предстательной железы. Применение ультразвукового метода для диагностики состояния предстательной железы было впервые описано в литературе Takahashi и Ouchi в Японии в 1963 году, и стало активно применяться в медицине лишь с 60-х годов прошлого столетия. В те годы применение ультразвукового метода для исследования простаты подавало большие надежды на значительное повышение качества диагностики РПЖ. В 1981 году Greenberg et al. впервые было отмечено, что для наличия аденокарциномы на ультразвуковых изображениях характерно появление очаговых зон с неправильными контурами повышенной либо сниженной эхогенности. Впоследствии, наличие признака гипоэхогенности опухолевых очагов было выявлено и другими авторами.
Однако в более поздних работах было показано, что признак гипоэхогенности не является абсолютно достоверным критерием для участков опухолевого поражения. Например, опухолевые участки небольших размеров чаще бывают гипоэхогенными, при увеличении их размеров эхогенность опухоли повышается, что затрудняет их поиск в серошкальном режиме. Так, в 2004 году Onur et al. было убедительно продемонстрировано, что частота выявляемости клеток аденокарциномы из гипоэхогенных участков и изоэхогенных зон практически идентична (9, 3% и 10, 4% соответственно). При расположении опухоли в центральной части и переходной зоне простаты, эхогенность опухолевого участка часто сопоставима с эхогенностью аденоматозно измененной ткани, что значительно затрудняет ее визуализацию. Исследование возможностей ТРУЗИ в В-режиме в диагностике РПЖ показывает его низкую специфичность (55-63%) и низкий ОПТ (52-60%). На основании приведенных данных, можно полагать, что низкая информативность ТРУЗИ в режиме серой шкалы обусловлена трудностями определения характера выявляемого патологического участка предстательной железы и визуализации изоэхогенных участков РПЖ.
Применение методики ультразвуковой ангиографии (ТРУЗИ-ангиография) повышает диагностическую и дифференциально-диагностическую ценность исследования в В-режиме, позволяя помимо выявления гипоэхогенных участков получать изображения кровеносных сосудов. Среди методик УЗ-ангиографии применяют цветовое допплеровское картирование (ЦДК), энергетическое картирование (ЭК), трехмерную ультразвуковую ангиографию (УЗ-ангиографию).
Режим ЦДК позволяет определить скорость и направление кровотока, однако не является высокоинформативным в связи с отсутствием возможности регистрировать мелкие сосуды с низкой скоростью кровотока, а также выявлять участки гиперваскуляризации при доброкачественных процессах, таких, как острый простатит. В связи с этим, для диагностики заболеваний простаты чаще используется метод ЭК, который обладает более высокой чувствительностью по сравнению с ЦДК, и позволяет визуализировать мелкие сосуды в структуре различных образований и участков.
Методика трехмерной ультразвуковой ангиографии впервые в отечественной литературе была описана в работах Зубарева А. В. и Гажоновой В. Е. Авторами было убедительно показано, что использование режима трехмерной реконструкции сосудистого рисунка позволяет заподозрить наличие опухоли при отсутствии изменений в В-режиме, точнее оценить размеры опухоли и наличие инвазии в капсулу железы, а также успешно применяться при динамическом наблюдении у пациентов с РПЖ и простатитами. Чувствительность ТРУЗИ с ЭК в диагностике РПЖ повышается до 86%, а в режиме ЭК с трехмерной ангиографией – до 90%.
Соноэластография (СЭГ) является еще одной ультразвуковой методикой, которая недавно широко вошла в практику при обследовании пациентов с различными изменениями предстательной железы. Первые экспериментальные научные работы по оценке эластичности и механических свойств тканей ПЖ у собак и человека (в норме и при злокачественном поражении) относятся к 1990-1993 гг.
Уже в 2001 году появилось первое (не экспериментальное) исследование, посвященное разработке значения модуля Юнга (модуля упругости, получаемого до и после деформации тканей) для неизмененной ПЖ, при ДГПЖ и раке ПЖ у человека. Первое клиническое исследование по применению СЭГ для диагностики РПЖ было опубликовано в 2002 году Cochlin et al. Авторами была произведена сравнительная оценка результатов СЭГ и стандартного серошкального ультразвука у 100 пациентов с подозрением на РПЖ. В результате проведенного исследования, чувствительность соноэластографии составила 51%, и практически не отличалась от чувствительности В-режима (54%), однако специфичность СЭГ оказалась выше, чем при исследовании в В-режиме (83% и 73% соответственно).
На сегодняшний день выделяют два метода СЭГ – статический и динамический. Получение соноэластографического изображения при статическом методе СЭГ основано на оказании компрессионного воздействия на ткани, при динамическом методе – базируется на вибрационном воздействии на ткани при помощи внешних источников (т. н. эластография сдвиговой волны). Наибольшее распространение получила методика статической, компрессионной СЭГ, благодаря относительной быстроты и простоты выполнения. Неоспоримым достоинством методики соноэластографии сдвиговых волн является меньшая зависимость получаемых результатов от практического опыта исследователя, а также возможность получения не только качественных, но и количественных показателей. Панфиловой Е. А. и соавт. базовая классификация соноэластографических изображений была адаптирована для заболеваний предстательной железы; были выделены основные типы картирования, характерные для доброкачественных и злокачественных изменений простаты. Согласно приведенным авторами данным, включение СЭГ в диагностический комплекс достоверно повышало специфичность традиционного ультразвукового исследования с 65, 4 до 78, 2% (p<0, 001), точность с 67, 3 до 78, 8% (p<0, 001), ППТ с 48, 1 до 62, 2% (p<0, 001). Помимо этого, авторы пришли к выводу, что применение СЭГ позволяет осуществлять дифференциальную диагностику РПЖ и воспалительных изменений, однако не может достоверно дифференцировать рак на фоне аденоматозных изменений центральной части простаты. Согласно данным источников литературы, чувствительность СЭГ в диагностике заболеваний ПЖ составляет от 74 % до 96 % и характеризуется значительной вариабельностью среди различных авторов.
Гистосканирование предстательной железы – еще одна новейшая неинвазивная ультразвуковая технология, которая позволяет выявить наличие рака в предстательной железе с помощью компьютерного анализа отраженных нативных УЗ-сигналов от клеток по всему объему железы. Гистосканирование является основанной на ультразвуковой методике технологией, что обуславливает такие преимущества ультразвука, как его простота, быстрота получения диагностического результата и отсутствие лучевой нагрузки, неинвазивность. Во время исследования на экране монитора отображаются различные срезы предстательной железы, визуализация которых позволяет более четко судить о локализации измененных участков, подозрительных в отношении опухолевого процесса; а также трехмерная модель простаты, что позволяет определить локализацию участков в пространственном отображении. При этом имеется возможность одновременного сопоставления локализации патологических участков с изменениями, выявленными при серошкальной эхографии в режиме реального времени. Система аппарата представляет также новый эффективный навигационный инструмент для выполнения биопсий предстательной железы, когда при помощи специального программного обеспечения под компьютерной навигацией и посрезового анализа ультразвуковых данных, биопсии выполняются прицельно из подозрительных участков. Использование этой функции позволяет увеличить точность позиционирования биопсийной иглы при выполнении инвазивных процедур. Метод позволяет осуществлять контроль на разных этапах лечения пациентов. В настоящее время проводятся соответствующие диагностические исследования по применению гистосканирования при лечении высокоинтенсивным фокусированным ультразвуком (HIFU) и брахитерапии рака предстательной железы.
Ультразвуковое исследование предстательной железы с эхоконтрастированием относится к малоизученным методикам. Эхоконтрастные препараты в диагностике РПЖ стали использовать в 1998 году, что явилось важным моментом в развитии ультразвукового метода. С помощью внутривенно вводимого эхоконтрастного вещества стало возможным изучать перфузию органа, визуализировать мельчайшие сосудистые структуры и даже исследовать ангиогенез. Первые результаты применения эхоконтрастных препаратов при обследовании пациентов с РПЖ были опубликованы Halpern et al. в 2000 году, однако исследование включало в себя малую группу пациентов, состоящую всего из 26 человек. Позже этими же авторами, уже в 2012 году, было представлено еще одно исследование. Оно включало в себя большую группу наблюдений, по результатам которого были показаны значительные преимущества использования эхоконтрастного ультразвукового исследования по сравнению с другими ультразвуковыми методиками при выявлении опухолей с суммой баллов по Глисону 7 и более. Аналогичные выводы были показаны в исследовании Frauscher et al.: применение эхоконтрастного ультразвукового исследования позволило выявить 27% случаев РПЖ среди 84 обследованных пациентов, тогда как исследование в В-режиме – 20% (р < 0. 05). Эхоконтрастная ангиография внесла значительный вклад в повышение информативности метода ТРУЗИ в диагностике РПЖ, позволяя повысить чувствительность с 89 до 94%, специфичность с 86 до 96%, точность с 88 до 95%. Использование эхоконтрастных препаратов при ультразвуковом исследовании простаты повышает процент выявляемости опухолевых очагов, но чувствительность и специфичность этой методики недостаточно высоки.
Метод компьютерной томографии (КТ) в основном используется для оценки состояния предстательной железы и окружающих ее органов и тканей, так как применение этого исследования для диагностики рака простаты ограничено. На компьютерных томограммах предстательная железа имеет однородную мягкотканную плотность, и ее дифференциация с окружающими тканями низкая. В связи с этим, по данным КТ невозможно четко дифференцировать злокачественное поражение простаты от доброкачественного, а также достоверно оценить распространенность процесса.
Основная роль КТ заключается в оценке состояния лимфатических узлов малого таза и брюшной полости, поэтому проведение этого исследования нецелесообразно у пациентов с уровнем общего ПСА менее 20 нг/мл ввиду низкой вероятности лимфогенного метастазирования у данных пациентов.
В настоящее время одним из лучших неинвазивных методов визуализации для обнаружения рака простаты считается магнитно-резонансная томография (МРТ). При МРТ качество отображения мягкотканных структур более высокое, чем при КТ. Это позволяет использовать данный метод на всех этапах проведения диагностики, стадирования опухоли, а также последующего лечения пациентов.
Использование T2 взвешенных изображений позволяет визуализировать морфологические изменения структуры предстательной железы. Главная диагностическая проблема при использовании Т2 взвешенных изображений заключается в отсутствии специфичности при визуализации различных, но морфологически сходных изменений ткани простаты. В то же время, отсутствие патологических очагов в железе при МРТ не исключает наличие опухолевого процесса. В периферической зоне часто выявляются участки сниженного МР-сигнала, вызванного различными доброкачественными заболеваниями. К подобным изменениям могут относиться, например, поствоспалительные или постбиопсийные рубцовые изменения, атрофические изменения, острый простатит, наличие участков интраэпителиальной неоплазии (ПИН) или изменения структуры тканей после проведенного гормонального или лучевого лечения. Таким образом, очаговые изменения, специфичные для опухолевого поражения, визуализируемые на T2 взвешенных изображениях, трудноотличимы от диффузных воспалительных изменений, вызванных хроническим либо острым простатитом. Так, гранулематозный простатит может быть представлен на Т2 взвешенных изображениях как гипоинтенсивный очаг, точно также будет выглядеть участок РПЖ. Определенные трудности при интерпретации МР-изображений встречаются при обследовании пациентов, которым незадолго до исследования ( 3-6 месяцев) были выполнены биопсийные вмешательства. Участки кровоизлияния и рубцовые изменения после выполнения биопсий также выглядят гипоинтенсивными на Т2 взвешенных изображениях, и гиперинтенсивными на Т1. При этом вероятность обнаружения рака в таких случаях снижается с уменьшением размера очагов поражения. Помимо этого, диагностика рака может быть затруднена при проведении МРТ у пациентов старше 50-ти лет, у которых присутствует ДГПЖ, особенно при локализации опухолевых очагов в центральной части железы.
Таким образом, данные литературы свидетельствует, что основным недостатком МРТ считается низкая специфичность в отношении выявления гипоинтенсивных участков в периферической части железы на Т2 взвешенных изображениях. Так, по данным Матякина Г. Г. и соавт. , чувствительность МРТ в оценке участка опухоли в предстательной железе составляет 72%.
Наряду с этим, важным преимуществом методики МРТ является ее стандартизированность. В 2011 году группой экспертов Европейской Ассоциацией Урогенитальной Радиологии были представлены рекомендации по проведению МРТ простаты, структуризации и стандартизации протоколов исследования по классификации PI-RADS, включающей в себя 5 градаций от 1 до 5.
Результаты МРТ в диагностике заболеваний предстательной железы на сегодняшний день являются весьма перспективными и многообещающими и, несомненно, улучшатся с появлением более мощных магнитов, использованием эндоректальных катушек и оптимизации изображений. Использование комбинации современных технологий МРТ, или мультипараметрической МРТ (мпМРТ), имеет большие перспективы в повышении диагностики РПЖ. К методикам мпМРТ относятся Т2 диффузионно-взвешенные изображения с построением карт измеряемого коэффициента диффузии и динамической МРТ с контрастным усилением и протонная магнитно-резонансная спектроскопия.
Например, сочетание традиционных Т1 и Т2 взвешенных изображений с динамической МРТ с контрастным усилением позволяет с большей точностью выявлять участки РПЖ, при сравнении с традиционным МРТ-исследованием. Применение МР-спектроскопии может повысить специфичность традиционной МРТ простаты, помимо этого позволяя произвести оценку степени агрессивности опухоли, а также быть использовано при динамическом наблюдении за пациентами в процессе лечения гормональной терапии.
В последние годы комплексный подход к диагностике рака простаты, включающий применение МРТ, ТРУЗИ с эхоконтрастированием, эластографии, гистосканирования обеспечил значительное улучшение качества диагностики этого заболевания. Однако, на сегодняшний день, несмотря на значительные достижения различных методик диагностики рака простаты, ни одна из них не обладает настолько высокими показателями чувствительности, специфичности и точности, чтобы можно было рассматривать их как альтернативу выполнению биопсийного исследования. Компьютер-ассистированные методики визуализации, основанные на построении трехмерных изображений, и т. н. «фьюжн» технологии, являются наиболее перспективными и предоставляют многообещающие возможности в объективизации диагностики РПЖ.
* Фёдорова А.А. "Возможности методики гистосканирования в диагностике рака предстательной железы" Дисс. канд. мед. наук М. 2015
1 октября 2017 г.
Ещё больше полезной информации на нашем Телеграм-канале