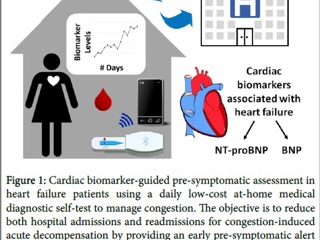
Доклиническая (предсимптомная) оценка сердечного биомаркера для диагностики застойных явлений у пациентов с сердечной недостаточностью с ежедневным использованием недорогой аппаратуры в домашних условиях. Цель состоит в том, чтобы уменьшить как госпитализацию, так и увеличить сроки ремиссии у пациентов с возможной острой декомпенсацией сердечной недостаточности путем ранней предсимптомной диагностики нарастания застойных явлений при лабораторном мониторинге уровня сердечных биомаркеров.
Хроническая сердечная недостаточность (СН) является основной причиной заболеваемости и смертности во всем мире. В Соединенных Штатах в настоящее время у 5, 8 миллиона человек диагностируется СН и Американская кардиологическая ассоциация прогнозирует, что к 2030 году более 8 миллионов американцев будут страдать от сердечной недостаточности. В Соединенных Штатах ежегодно госпитализируется 1 миллион пациентов, у которых ранее была диагностирована СН, в результате чего примерно 34 миллиарда долларов ежегодно расходуется на лечение пациентов с сердечной недостаточностью только в Соединенных Штатах, причем ~ 70% ежегодных расходов приходится на неотложную стационарную помощь. Из 1 миллиона пациентов, ежегодно госпитализируемых по поводу СН, примерно 25% также повторно поступают в течение 30 дней после выписки, что приводит к дополнительным затратам на госпитализацию в размере 2, 7 миллиарда долларов в год.
Основной причиной, как первичной, так и повторной госпитализацией пациентов с ранее диагностированной СН, является острая декомпенсация, вызванная застойными изменениями внутренних органов. Начало клинической картины, требующей госпитализации, может быть незначительным, с субклиническими проявлениями за несколько дней или недель до возникновения острой манифестации, часто начинающейся внезапно. Это наблюдение предполагает, что раннее лечение субклинических проявлений СН до того, как она станет острой, потенциально может снизить как начальную госпитализацию, так и частоту повторной госпитализации у многих пациентов с СН.
Нынешний стандарт медицинской помощи для лечения застойных явлений у пациентов с сердечной недостаточностью включает в себя домашний контроль, последовательный самоконтроль веса, тщательное регулирование объема водного баланса, прием лекарств, которые улучшающих отдаленные результаты при сердечной недостаточности, в сочетании с личными визитами к врачу. К сожалению, это недостаточно для своевременной корректировки терапевтической помощи до тех пор, пока у пациентов не появятся выраженные симптомы. Как только проявляются симтомы застойной СН, пациенты нуждаются в госпитализации. Существует быстро растущее признание потенциала циркулирующих биомаркеров сердца для помощи в предсимптомной оценке и проактивном лечении застойных явлений у пациентов с СН. Независимо от первоначальной причины застойной сердечной недостаточности, нарушение работы миокарда приводит к ряду компенсаторных механизмов, связанных с биомаркерами, которые могут отражать застойное состояние. Наиболее исследоваными из этих клинически доказанных биомаркеров сердца являются натрийуретический пептид B-типа (BNP) и близкородственный N-концевой фрагмент его прогормона, NT-proBNP, которые высвобождаются при растяжении стенки желудочка, вызывая расширение сосудов и ингибирование ренина -ангиотензиновой системы
Было проведено множество клинических испытаний, демонстрирующих диагностическую полезность мониторинга BNP у пациентов с СН. В одном из исследований уровни BNP в пределах 100 пг / мл, имели чувствительность 90% и специфичность 73% для диагностики сердечной недостаточности у пациентов, госпитализированных с острой одышкой. Повышенный уровень BNP, является наиболее точным предиктором для выявления и дифференциации застойной сердечной недостаточности от других причин острой одышки. В других исследованиях уровни BNP> 300 пг / мл пациента были прогностически не благоприятны как для выписки, так и в амбулаторных условиях. В амбулаторном мониторинговом исследовании было также показано, что как рутинные, так и повторные измерения BNP с использованием целевого порога ~ 125 пг / мл снижают риск декомпенсации сердечной недостаточности. Тем не менее, одна из слабых сторон этих исследований заключается в том, что уровни биомаркеров сердечного натрийуретического пептида (NP) измерялись слишком редко. Кроме того, ингибитор неприлизина рецептора ангиотензина II сакубитрил-валсартан (Entresto®), который в настоящее время становится общепринятым при сердечной недостаточности, приводит к устойчивому уровню BNP в кровотоке пациента, в то время как сакубитрил не влияет на NT-proBNP. Это говорит о том, что в перспективе предпочтительней исследовать уровень биомаркера NT-proBNP, а не BNP.
Учитывая потенциальную клиническую пользу более частого амбулаторного мониторинга BNP или NT-proBNP для своевременной коррекции терапии у пациентов с СН необходимо разработать подходы для возможного серийного домашнего тестирования.
Исследование HABIT было недавним пилотным исследованием у 163 пациентов с сердечной недостаточностью, в котором оценивались ежедневные измерения уровня BNP в крови в домашних условиях в течение первых 60 дней после выписки. Это исследование показало, что ежедневное отслеживание уровней биомаркеров BNP и определение их тенденций было лучшим показателем прогноза у пациентов с СН, чем оценка однократного абсолютного уровня BNP при выписке, а также являлось потенциально полезным методом мониторинга ранней декомпенсации. Тем не менее, в настоящее время в США нет утвержденных FDA самодиагностических тестов на сердечные биомаркеры NP. Вместо этого пациентам с сердечной недостаточностью необходимо посетить клинику или диагностическую лабораторию для тестирования серийных биомаркеров NP.
В настоящее время интенсивный мониторинг биомаркеров сердца еще не продемонстрировал достоверного влияния на клинические исходы, но, по-видимому, требует дальнейшей оценки. При правильной диагностической технологии пациенты с сердечной недостаточностью могут регулярно измерять и отслеживать уровни циркулирующего биомаркера BNP или NT-proBNP с помощью анализа крови из пальца, что на практике аналогично результатам самоконтроля уровня глюкозы в крови, используемого сегодня диабетиками. Этот тип портативного устройства самопроверки должен быть как простым в использовании, так и относительно недорогим, чтобы помочь пациентам с хронической сердечной недостаточностью справиться с застоем. Тем не менее, как технология молекулярной диагностики, так и технология электроники, используемая для измерения уровня глюкозы в крови в существующих недорогих домашних тестах для самостоятельного определения уровня глюкозы в крови, не достаточно чувствительна для рутинного отслеживания предсимптомных относительных уровней биомаркеров BNP или NT-proBNP у пациентов с СН.
Колориметрическая технология иммуноанализа, обычно используемая сегодня на тест-полосках в комплектах для самопроверки на беременность, включая новые цифровые версии с подключением к смартфону, может являться, в некотором роде аналогом для определения циркулирующего биомаркера СН вплоть до необходимых диапазонов. Хотя основными преимуществами технологии колориметрических тест-полосок для домашнего использования являются очень низкие производственные затраты в сочетании с простотой использования, низкая чувствительность серьезно ограничивает полезность колориметрических иммуноанализов для обеспечения предсимптомной оценки. Альтернатива, иммуноанализа на основе флуоресценции может значительно улучшить как чувствительность, так и количественный анализ по сравнению с существующей колориметрической технологией. В иммуноанализах на основе флуоресценции биораспознавания на тест-полоске активно окрашивается источником яркого света, а испускаемый флуоресцентный сигнал детектируется электронным способом с использованием чувствительной электроники считывания. Технология флуоресцентного биораспознающего иммуноанализа предлагает на два-три порядка более высокую аналитическую чувствительность по сравнению с колориметрией и, по прогнозам, обеспечит необходимую чувствительность в пг / мл. Однако обычные флуоресцентные диагностические инструменты на основе биораспознавания представляют собой относительно сложные и дорогие настольные машины, которые обычно требуют регулярного технического обслуживания, калибровки и очистки. Это делает их проблематичными для домашнего использования, поскольку они требуют, чтобы каждый пользователь (пациент) устанавливал эквивалент собственной диагностической лаборатории в своем доме.
Одним из потенциальных решений в домашних условиях является конфигурация, в которой сочетаются высокая чувствительность и количественный анализ настольных приборов на основе флуоресцентного биораспознования с общепризнанным удобством, простотой использования и низкой стоимостью колориметрических тест-полосок для иммуноанализа. При таком подходе колориметрическая метка просто заменяется флуоресцентной меткой на тест-полоске в сочетании с созданием недорогого, простого в использовании прибора для электронного обнаружения испускаемого флуоресцентного сигнала. На сегодняшний день общепризнанным ограничением в создании высокочувствительных флуоресцентных приборов для биологического распознавания является необходимость в больших и дорогих оптических компонентах, таких как оптические микроскопы, вместе с лазерами, фильтрами и цифровыми камерами при слабом освещении. Затем эти оптические компоненты должны быть объединены со сложной и дорогой электроникой считывания для электронного обнаружения испускаемых флуоресцентных сигналов.
В качестве потенциального решения этого ключевого ограничения, мы разработали недорогую прототипную конфигурацию для обнаружения низкоуровневых предсимптомных раковых биомаркеров, которая устраняет необходимость в отдельной увеличительной оптике, помещая флуоресцентный слой биораспознавания непосредственно между недорогим источником света и кремниевым фотодиодным детектором. Это не новая оптическая конфигурация; тем не менее, в нашем подходе мы решили проблему плохой диагностической чувствительности, о которой сообщалось ранее, путем объединения очень дешевых высококачественных фильтров оптического излучения / возбуждения с недорогой электроникой интеграции зарядов с нейроморфным эффектом. Мы продемонстрировали, что этот новый подход может обеспечить высокочувствительное количественное обнаружение флуоресцентного сигнала в требуемом диапазоне пг / мл, используя компактную конфигурацию, которая, как ожидается, будет схожа по стоимости с домашними глюкометрами, используемыми сегодня.
Ключевым новым пониманием стало признание того, что сегодня быстро развиваются IT технологии
3 июля 2019 г.
Источник: «Future Strategies for Managing Congestion in Heart Failure Patients Using Cardiac Biomarker-Guided Self-Testing» J Clin Exp Cardiolog 2017, Vol 8(10): 548 Joseph T. Smith, Uwadiae Obahiagbon, Radwa Ewaisha, Meilin Zhu, Matthew F.A. McFadden, Jennifer M. Blain Christen, Anantharam Kalya, Alexandra R. Lucas and Karen S. Anderson Joseph T. Smith
Ещё больше полезной информации на нашем Телеграм-канале