Закарян Н.В., Панков А.С.
Современные исследования показывают, что открытые хирургические вмешательства при торакоабдоминальных аневризмах аорты (TAAA) в центрах с большим опытом работы могут быть выполнены с удовлетворительными результатами [45-51]. Наиболее часто анализируются показатели летальности и ишемии спинного мозга, другими важными конечными точками исследований являются развитие почечной недостаточности, качество жизни, и функциональный статус пациента после операции.
Coselli с соавторами сообщили о 2286 пациентах, которым была выполнена открытая коррекция TAAA, при этом операционная смертность составила 6,6%, а частота повреждений спинного мозга - 4% [45]. В других крупных центрах показатели смертности при подобных операциях колебались в диапазоне от 4,6% до 14,6% [47-51]. Тем не менее, реальные данные при оценке национальных и региональных регистров демонстрирует более пессимистические результаты. Так, в исследовании, проведенном Rigberg, были изучены данные базы Medicare в Калифорнии, согласно которым после проведения открытых хирургических вмешательств при ТААА у 797 пациентов частота летальности в течение 30 дней после операции составила 19%, а в течение 1 года - 31%. [46].
В течение последнего десятилетия развивались активно эндоваскулярные методы коррекции TAAA. Первичные данные по использованию фенестрированных эндографтов и многобраншевых графтов (протезов со вшитыми висцеральными ветвями), показали, что тотальное эндоваскулярное протезирование аорты может снизить частоту осложнений у больных с наличием протяженных торакоабдоминальных анервизм, по сравнению с результатами открытых вмешательств [52]. Тем не менее, эти устройства более дороги, не всегда доступны (требуется очень точный расчет всех размеров специально под пациента) и достаточно сложны при их имплантации. Кроме того, пока еще нет отдаленных результатов клинических исследований, выполненных на большом количестве больных, которые бы узаконили подобную стратегию.
Из-за отсутствия широко доступных фабричных конструкций сложных эндографтов, специалисты разрабатывали творческие методы эндопротезирования торакоабдоминальных аневризм с вовлечением висцеральных ветвей, например, методики “дымоход” (“chimney”), “сэндвич”(“sandwich”), “осьминог”(“octopus”) и др. [43]. Тем не менее, применение в практике таких операций часто ограничено вследствие отсутствия контроля качества, нарушения основных биоинженерных концепций эндопротезирования, а также спорной продолжительностью их адекватного функционирования в будущем.
Гибридные вмешательства при лечении торакоабдоминальных аневризм стали использоваться в качестве менее инвазивной альтернативы традиционной открытой хирургии. Они часто позволяют избежать торакотомии, пережатия аорты и длительной ишемии органов-мишеней. Первое подобное вмешательство было выполнено Quinones-Baldrich c коллегами из Калифорнийского университета в 1999 году [49]. В настоящее время подобные операции применяются все чаще у пациентов с высоким хирургическим риском проведения открытых операций, которые в то же время не являются идеальными кандидатами на тотальное эндоваскулярное протезирование.
Одним из главных принципов эндоваскулярного лечения аневризм является наличие адекватной зоны фиксации стент-графта. Гибридное вмешательство должно рассматриваться только в случае, если экстра-анатомическое шунтирование обеспечит надлежащую проксимальную и/или дистальные зоны фиксации эндопротеза.
В большинстве центров перед планированием вмешательства используют КТ-ангиографию в качестве оптимального метода визуализации; реже используется магнитно-резонансная ангиография [45-53]. Наличие конусовидной, кальцинированной и ангулированной шейки аневризмы компрометирует адекватное прикрепление графта. В грудной аорте необходимая длина зоны проксимальной фиксации должна быть не меньше 2 см, также в этом участке стенки аорты не должно быть тромба или сильного кальциноза. Дистальная фиксация устройства осуществляется в общих подвздошных артериях, инфраренальной аорте, или в ранее установленном аортальном графте, и также является очень важной составляющей общего успеха. Если общие подвздошные артерии аневризматически расширены, сохранение кровотока в малом тазу имеет решающее значение для минимизации риска развития ишемии спинного мозга [45-50]. Ветви аорты, отходящие от аневризмы, должны быть тщательно изучены на предмет наличия значимых сужений, выраженного кальциноза или тромбоза, а также необычной или аберрантной анатомии. Например, при кальцинозе, малом диаметре почечных артерий или при наличии нескольких почечных артерий может потребоваться обширная хирургическая реконструкция.
Особенно тщательно должно быть оценено место проксимального анастомоза основного шунта для висцеральных артерий, которое, как правило, находится в дистальной части общей подвздошной, либо проксимальной части наружной подвздошной артерии. В случае отсутствия значимого атеросклероза данной зоны можно рассчитывать на оптимальный приток крови к шунтированным артериям. Также нужно внимательно оценить анатомию венозной системы, т.к. наличие какой-либо венозной аномалии (например, левостороннее расположение нижней полой вены, ретроаортальная позиция почечной вены и т.д.) может привести к случайному повреждению крупной вены в ходе шунтирования. Наконец, очень важно убедиться в хорошем состоянии подвздошной артерии, по которой будет продвигаться основная часть стент-графта . Противоположная подвздошная артерия при этом обычно используется для наложения шунта к висцеральным артериям, который укладывается в забрюшинном пространстве в рамках подготовки ко второму этапу вмешательства.
Технические особенности торакоабдоминального дебранчинга.
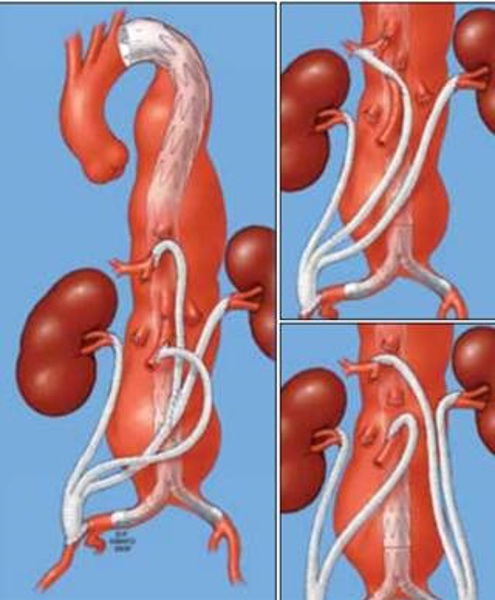
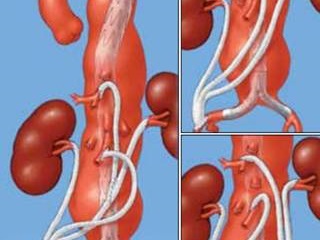
Операция обычно начинается со срединного чрезбрюшинного или забрюшинного доступа, и выполняется одномоментно или в 2 этапа. При двухэтапном подходе можно уменьшить частоту осложнений и летальности, особенно у пациентов высокого риска или у тех, кто нуждается в сложной открытой хирургической реконструкции. Тем не менее, одномоментные гибридные операции исключают риск разрыва аневризмы между этапами и должны выполняться у больных без сложного варианта дебранчинга, у пациентов с большой протяженной аневризмой, а также в случаях, когда требуется более ограниченная протяженность покрытия аорты стент-графтом [47-54]. Обычно проксимальную часть шунта для висцеральных артерий анастомозируют с дистальным сегментом общей подвздошной, либо проксимальным сегментом наружной подвздошной артерии. Так, в работе Oderich показано, что в большинстве случаев использовался трифуркационный шунт, исходящий из общей подвздошной артерии, ветви которого потом вшивались в почечные артерии, в ветви чревного ствола, а также в брыжеечные артерии (в случае необходимости к этому шунту добавлялись еще 1-2 висцеральных протеза) [48]. Также описаны варианты, когда главный шунт отходил от инфраренальной аорты, от ранее имплантированного графта, а также от печеночной или селезеночной артерии. Некоторые варианты использования дебранчинга при торакоабдоминальных аневризмах представлены на рис. 1.
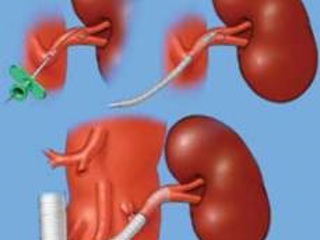
Интересная техника дебранчинга под названием VORTEC (рис. 2), была описана Lachat и соавт. в 2008 году [55]. После выполнения открытого доступа проводится прямая пункция почечной артерии (на брыжеечных артериях или чревном стволе указанная техника используется реже). Далее по методике Селдингера в почечную артерию доставляется стент-графт “Viabahn” фирмы Gore & Associates, и раскрывается частично внутри артерии, частично – снаружи. Для прочной фиксации графта в почечной артерии накладывают несколько швов. Далее формируется анастомоз по типу “конец в бок” c протезированной аортой, проксимальная часть почечной артерии перевязывается для предотвращения эндолика. Указанная методика позволяет снизить время ишемии почек и других органов по сравнению с классическими вмешательствами [55].
По данным регистра North American Complex Abdominal Aortic Debranching (NACAAD) были проанализированы результаты гибридных вмешательств у 208 пациентов с торакоабдоминальными аневризмами (одноэтапно операции выполнялись у 92 больных, двухэтапно – у 116 пациентов) [48]. У всех пациентов использовались разные виды дебранчинга для переключения 1-4 висцеральных артерий. 30-дневная летальность в среднем составила 14% (у больных с высоким хирургическим риском – 17%, с низким риском – 3%). Предикторами ранней летальности в данном регистре явились наличие сопутствующей коронарной патологии, выраженной сердечной недостаточности, хронической почечной недостаточности, высокий операционный риск, а также выполнение дебранчинга сразу 4-х висцеральных артерий. Ишемия спинного мозга развилась у 10%, ишемический колит – у 6% пациентов. Выживаемость через 3 и 5 лет составила 77% и 61% соответственно. Первичная проходимость графтов через 1 год составила 90% [48]. Для улучшения результатов авторы рекомендуют применять селективную перфузию висцеральных артерий с целью защиты органов-мишеней.
Суммируя все вышесказанное, гибридные операции позволяют уменьшить риски развития осложнений и летальных исходов у пациентов с многоэтажными поражениями периферических артерий, а также у больных со сложными анатомическими вариантами аневризм и расслоений любых отделов аорты. Разработка новых стент-графтов и операционных методик, а также накопление опыта позволит уже в ближайшем будущем увеличить частоту выполнения гибридных вмешательств и улучшить их результаты во всем мире.
Список литературы:
- Antoniou GA, Sfyroeras GS, Karathanos C, et al. Hybrid endovascular and open treatment of severe multilevel lower extremity arterial disease // Eur J Vasc Endovasc Surg. – 2009. – Vol. 38(5). – P. 616–622.
- Balaz P, Rokosny S, Bafrnec J, Björck M. The role of hybrid procedures in the management of peripheral vascular disease // Scand J Surg. – 2012. – Vol. 101(4). – P. 232–237.
- Chang RW, Goodney PP, Baek JH, Nolan BW, Rzucidlo EM, Powell RJ. Long-term results of combined common femoral endarterectomy and iliac stenting/stent grafting for occlusive disease // J Vasc Surg. – 2008. – Vol. 48(2). – P. 362–367.
- Cotroneo AR, Iezzi R, Marano G, Fonio P, Nessi F, Gandini G. Hybrid therapy in patients with complex peripheral multifocal steno-obstructive vascular disease: two-year results // Cardiovasc Intervent Radiol. – 2007. – Vol. 30(3). – P. 355–361.
- Dosluoglu HH, Cherr GS. Pre-arteriotomy guidewire access (PAGA): a crucial maneuver for securing infow and/or outfow in patients with bulky iliofemoral occlusive disease undergoing combined (open/endovascular) procedures // Eur J Vasc Endovasc Surg. – 2006. – Vol. 32(1). – P. 97–100.
- Dosluoglu HH, Lall P, Cherr GS, Harris LM, Dryjski ML. Role of simple and complex hybrid revascularization procedures for symptomatic lower extremity occlusive disease // J Vasc Surg. – 2010. – Vol. 51(6). – P. 1425–1435.
- Ebaugh JL, Gagnon D, Owens CD, Conte MS, Raffetto JD. Comparison of costs of staged versus simultaneous lower extremity arterial hybrid procedures // Am J Surg. – 2008. – Vol. 196(5). – P. 634–640.
- Schanzer A, Owens CD, Conte MS, Belkin M. Superficial femoral artery percutaneous intervention is an effective strategy to optimize inflow for distal origin bypass grafts // J Vasc Surg. – 2007. – Vol. 45. – P. 740–743.
- Lyden SP, Smouse HB. TASC II and the endovascular management of infrainguinal disease // J Endovasc Ther. – 2009. – Vol. 16(2). – P. II5–II18.
- Matsagkas M, Kouvelos G, Arnaoutoglou E, Papa N, Labropoulos N, Tassiopoulos A. Hybrid procedures for patients with critical limb ischemia and severe common femoral artery atherosclerosis // Ann Vasc Surg. – 2011. – Vol. 25(8). – P. 1063–1069.
- Joh J. et al. Simultaneous hybrid revascularization for symptomatic lower extremity arterial occlusive disease // Experimental and therapeutic medicine. – 2014. – P. 804-810.
- Schneider P., Caps M., Ogawa D. Intraoperative superficial femoral artery balloon angioplasty and popliteal to distal bypass graft: an option for combined open and endovascular treatment of diabetic gangrene // J Vasc Surg. – 2001. – Vol. 33. – P. 955–962.
- Nishibe T, Kondo Y, Dardik A, Muto A, Koizumi J, Nishibe M. Hybrid surgical and endovascular therapy in multifocal peripheral TASC D lesions: up to three-year follow-up // J Cardiovasc Surg (Torino). – 2009. – Vol. 50(4). – P. 493–499.
- Piazza M, Ricotta JJ II, Bower TC, et al. Iliac artery stenting combined with open femoral endarterectomy is as effective as open surgical reconstruction for severe iliac and common femoral occlusive disease // J Vasc Surg. – 2011. – Vol. 54(2). – P. 402–411.
- Reed AB. Endovascular as an open adjunct: use of hybrid endovascular treatment in the SFA // Semin Vasc Surg. – 2008. – Vol. 21(4). – P. 200–203.
- Van Den Berg J, Waser S, Trelle S, Diehm N, Baumgartner I. Lesion characteristics of patients with chronic critical limb ischemia that determine choice of treatment modality // J Cardiovasc Surg (Torino). – 2012. – Vol. 53(1). – P. 45–52.
- Scali ST, Rzucidlo EM, Bjerke AA, et al. Long-term results of open and endovascular revascularization of superfcial femoral artery occlusive disease // J Vasc Surg. – 2011. – Vol. 54(3). – P. 714–721.
- Schrijver AM, Moll FL, De Vries JP. Hybrid procedures for peripheral obstructive disease // J Cardiovasc Surg (Torino). – 2010. – Vol. 51(6). – P. 833–843.
- Reed AB. Hybrid procedures and distal origin grafts // Semin Vasc Surg. – 2009. – Vol. 22(4). – P. 240–244.
- Fernandez N, McEnaney R, Marone LK, et al. Multilevel versus isolated endovascular tibial interventions for critical limb ischemia // J Vasc Surg. – 2011. – Vol. 54(3). – P. 722–729.
- Karathanos C, Sfyroeras GS, Stamoulis K, Drakou A, Vretzakis G, Giannoukas AD. Hybrid procedures for the treatment of multi-focal ipsilateral internal carotid and proximal common carotid or innominate artery lesions // Vasa. – 2011. – Vol. 40. – P. 241–245
- Bazan H, Sheahan M, Dardik A. Carotid endarterectomy with simultaneous retrograde common carotid artery stenting: Technical considerations // Catheter Cardiovasc Interv. – 2008. – Vol. 72. – P. 1003–1007.
- Zhang L., Xing T. et al. Preliminary application of hybrid operation in the treatment of carotid artery stenosis in patients with complex ischemic cerebrovascular diseases // Int J Clin Exp Pathol. – 2014. – Vol. 7(8). – P. 5355–5362
- Czerny M, Weigang E, Sodeck G, et al. Targeting landing zone 0 by total arch rerouting and TEVAR: midterm results of a transcontinental registry // Ann Thorac Surg. – 2012. – Vol. 94. – P. 84-89.
- Donas KP, Rancic Z, Lachat M, et al. Novel sutureless telescoping anastomosis revascularization technique of supra-aortic vessels to simplify combined open endovascular procedures in the treatment of aortic arch pathologies // J Vasc Surg. – 2010 – Vol. 51. – P. 836-841.
- Andersen ND, Williams JB, Hanna JM, et al. Results with an algorithmic approach to hybrid repair of the aortic arch // J Vasc Surg. – 2013. – Vol. 57. – P. 655-667.
- Ferrero E, Ferri M, Viazzo A, et al. Is total debranching a safe procedure for extensive aortic-arch disease? // Eur J Cardiothorac Surg. – 2012. – Vol. 41. – P. 177-182.
- Mitchell RS, Ishimaru S, Ehrlich MP, et al. First International Summit on Thoracic Aortic Endografting: roundtable on thoracic aortic dissection as an indication for endografting // J Endovasc Ther. – 2002. – Vol. 9. – P. 98-105.
- Chiesa R, Melissano G, Tshomba Y, et al. Ten years of endovascular aortic arch repair // J Endovasc Ther. – 2010. – Vol. 17. – P. 1-11.
- Geisbüsch P, Kotelis D, Müller-Eschner M, et al. Complications after aortic arch hybrid repair // J Vasc Surg. – 2011. – Vol. 53. – P. 935-941.
- Deriu G, Grego F, Frigatti P, et al. Unusual inflow sources and device introduction sites in aortic arch debranching // J Cardiovasc Surg (Torino). – 2012. – Vol. 53. – P. 143-151.
- Чарчян Э.Р., Абугов С.А., Степаненко А.Б. и др. Гибридные операции при патологии грудной аорты // Клин. и эксперимент. хир. Журн. им. акад. Б.В. Петровского. - 2014. - № 4. - С. 31-36.
- Antoniou GA, Mireskandari M, Bicknell CD, et al. Hybrid repair of the aortic arch in patients with extensive aortic disease // Eur J Vasc Endovasc Surg. – 2010. – Vol. 40. – P. 715-721.
- Bavaria J, Milewski RK, Baker J, et al. Classic hybrid evolving approach to distal arch aneurysms: toward the zone zero solution // J Thorac Cardiovasc Surg. – 2010. – Vol. 140. – P. 77-80.
- Gelpi G, Vanelli P, Mangini A, et al. Hybrid aortic arch repair procedure: reinforcement of the aorta for a safe and durable landing zone // Eur J Vasc Endovasc Surg. – 2010. – Vol. 40. – P. 709-714.
- Holt PJ, Johnson C, Hinchliffe RJ, et al. Outcomes of the endovascular management of aortic arch aneurysm: implications for management of the left subclavian artery // J Vasc Surg. – 2010. – Vol. 51. – P. 1329-1338.
- Jakob H, Tsagakis K, Pacini D, et al. The International E-vita Open Registry: data sets of 274 patients // J Cardiovasc Surg (Torino). – 2011. – Vol. 52. – P. 717-723.
- Nishi H, Mitsuno M, Tanaka H, et al. Spinal cord injury in patients undergoing total arch replacement: a cautionary note for use of the long elephant technique // J Thorac Cardiovasc Surg. – 2011. – Vol. 142. – P. 1084-1089.
- Sun L, Qi R, Zhu J, Liu Y, et al. Total arch replacement combined with stented elephant trunk implantation: a new “standard” therapy for type a dissection involving repair of the aortic arch? // Circulation. – 2011. – Vol. 123. – P. 971-978.
- Borst HG, Walterbusch G, Schaps D. Extensive aortic replacement using “elephant trunk” prosthesis // Thorac Cardiovasc Surg. – 1983. – Vol. 31. – P. 37-40.
- Kawaharada N, Kurimoto Y, Ito T, et al. Hybrid treatment for aortic arch and proximal descending thoracic aneurysm: experience with stent grafting for second-stage elephant trunk repair // Eur J Cardiothorac Surg. – 2009. – Vol. 36. – P. 956-961.
- Lima B, Roselli EE, Soltesz EG, et al. Modified and “reverse” frozen elephant trunk repairs for extensive disease and complications after stent grafting // Ann Thorac Surg. – 2012. – Vol. 93. – P. 103-109.
- Shahverdyan R. et al. Triple-barrel Graft as a Novel Strategy to Preserve Supra-aortic Branches in Arch-TEVAR Procedures: Clinical Study and Systematic Review // Eur J Vasc and Endovasc Surg. – 2013. – Vol. 45 (1). – P. 28-35.
- Rango P. et al. Systematic review of clinical outcomes in hybrid procedures for aortic arch dissections and other arch diseases // J Thorac Cardiovasc Surg. – 2012. – Vol. 144(6). – P. 1286-1300.
- Coselli JS, Bozinovski J, LeMaireSA. Open surgical repair of 2286 thoracoabdominal aortic aneurysms // Ann Thorac Surg . – 2007. – Vol. 83. – P. 862–864.
- Rigberg D. et al. Thirty-day mortality statistics underestimate the risk of repair of thoracoabdominal aortic aneurysms: A statewide experience // J Vasc Surg. – 2006. – Vol. 43 (2). – P. 217-222.
- Moulakakis KG, Mylonas SN, Avgerinos E, et al. Hybrid open endovascular technique for aortic thoracoabdominal pathology // Circulation. – 2011. – Vol. 124. – P. 2670.
- Oderich GS, Gloviczki P, Farber M, et al. Abdominal debranching with aortic stent grafts for complex aortic aneurysms: preliminary results of the North American Complex Abdominal Aortic Debranching (NACAAD) Registry // Society for Vascular Surgery meeting; Chicago, IL; June 15-18, 2011.
- Quinones-Baldrich W, Jimenez JC, DeRubertis B, Moore WS. Combined endovascular and surgical approach (CESA) to thoracoabdominal aortic pathology: a 10-year experience // J Vasc Surg. – 2009. – Vol. 49. – P. 1125-1134.
- Patel HJ, Upchurch GR, Eliason JL, et al. Hybrid debranching with endovascular repair for thoracoabdominal aneurysms: a comparison with open repair // Ann Thorac Surg. – 2010. – Vol. 89. – P. 1475-1481.
- Drinkwater SL, Goebells A, Haydar A, et al. The incidence of spinal cord ischemia following thoracic and thoracoabdominal endovascular intervention // Eur J Vasc Endovasc Surg. – 2010. – Vol. 40. – P. 729-735.
- Safi HJ ,Estrera AL, Azizzadeh A,et al. Progress and future challenges in thoracoabdominal aortic aneurysm management // World J Surg. – 2008. – Vol. 32. – P. 355–360.
- Bakoyiannis C, Kalles V, Economopoulos K, et al. Hybrid techniques in the treatment of thoracoabdominal aortic aneurysms: systematic review // J Endovasc Ther. – 2009. – Vol. 16. – P. 443.
- Resch TA, Greenberg R, Lyden SP, et al. Combined staged procedures for the treatment of thoracoabdominal aneurysms // J Endovasc Ther. – 2006. – Vol. 13. – P. 481-489.
- Lachat M, Mayer D, Criado FJ, et al. New technique to facilitate renal revascularization with use of telescoping self-expanding stent grafts: VORTEC // Vascular. – 2008. – Vol. 16. – P. 69-72.
15 апреля 2016 г.
Ещё больше полезной информации на нашем Телеграм-канале