Обсуждаются основные вопросы хирургической тактики при больших и гигантских послеоперационных грыжах у пациентов старших возрастных групп. В результате анализа причин рецидивов грыжи, причин развития послеоперационных осложнений выявлена необходимость применения алгоритмизированного подхода к выбору метода пластики передней брюшной стенки, определены критерии возможности проведения оперативного пособия у пациентов с выраженной сопутствующей патологией, а также программа предоперационной подготовки.
Лечение пациентов пожилого и старческого возраста с большими и гигантскими послеоперационными вентральными грыжами (ПВГ) принято относить к числу наиболее сложных проблем современной герниологии. По мнению большинства авторов операции по поводу ПВГ у больных старших возрастных групп сопровождаются большим количеством послеоперационных осложнений (15-33%), высоким уровнем летальности (7-25%) и частым рецидивированием грыж (18-44%) [2,3]. В связи с этим больным старших возрастных групп с неущемленными ПВГ зачастую отказывают в плановом оперативном лечении, мотивируя это, прежде всего, наличием выраженной сопутствующей патологии, что в свою очередь приводит к закономерному возрастанию числа неотложных операций уже по поводу ущемленных ПВГ в данной возрастной группе.
По мнению большинства исследователей отдаленные результаты операции при ПВГ зависят от метода пластики дефекта передней брюшной стенки. При этом непосредственные результаты связаны с различной толерантностью больных старших возрастных групп к неизбежному повышению внутрибрюшного давления, возникающему при перемещении содержимого грыжевого мешка в брюшную полость и, тем более, при сведении краев грыжевых ворот [1]. Аутоаллопластика грыжевого дефекта, характеризуется наименьшим числом рецидивов грыжи, но в тоже время часто сопровождается нарушениями функции внешнего дыхания и оказывает значимое влияние на системную гемодинамику. Очевидно, что операции, проводимые пациентам старших возрастных групп по поводу ПВГ без соответствующей предоперационной подготовки, либо не являются адекватными для профилактики рецидива ПВГ, либо сопровождаются клинически значимыми нарушениями со стороны сердечно-сосудистой и дыхательной систем в послеоперационном периоде [5]. Для оптимизации лечебной тактики у пациентов старшей возрастной группы с ПВГ было проведено исследование, имевшее своими принципиальными задачами установление факторов, достоверно оказывающих влияние на возникновение рецидива заболевания, определение вариантов оперативных вмешательств, характеризующихся лучшими непосредственными и отдаленными результатами, разработка моделей натяжной и ненатяжной пластики для прогнозирования в предоперационном периоде толерантности пациентов к послеоперационному изменению внутрибрюшного давления, выявление факторов, ограничивающих возможность выполнения комбинированной аутоаллопластики у пациентов старших возрастных групп с обширными и гигантскими ПВГ. Непосредственной практической задачей являлась разработка алгоритма выбора метода оперативного вмешательства и составления программы предоперационной подготовки при лечении пациентов старших возрастных групп с обширными и гигантскими ПВГ.
На первом этапе исследования ретроспективному анализу были подвергнуты 198 клинических случая у пациентов пожилого и старческого возраста, оперированных по поводу ПВГ . При этом у 57 (29%) пациентов имели место обширные (по классификации В,В, Жебровского, 1990) грыжевые дефекты передней брюшной стенки, полностью занимавшие одну анатомическую область, у 141 (71%) пациента имели место гигантские грыжевые дефекты, занимавшие две, три и более анатомических областей (классификация В.В. Жебровского, 1990 г.). Все пациенты с ПВГ были оперированы в плановом порядке. 102 (51%) пациентам выполнена пластика грыжевого дефекта местными тканями, 96 (49%) пациентам была выполнена протезирующая аутоаллопластика грыжевого дефекта.
В раннем послеоперационном периоде местные послеоперационные осложнения имели место у 51% пациентов (серомы - 25%, нагноение послеоперационной раны - 26%). Системные послеоперационные осложнения развились у 25% пациентов (послеоперационная пневмония - 15%, инфаркт миокарда - 2%, ТЭЛА - 8%).
Отдаленные результаты у пациентов ретроспективной группы оказались следующими. Рецидив ПВГ (телефонный опрос, повторные госпитализации) в течение 3 лет выявлен у 43 (22%) из 198 пациентов. После проведенной пластики местными тканями рецидив ПВГ имел место у 38% пациентов. Протезирующая пластика передней стенки по методике on-lay сопровождалась возникновением рецидива ПВГ у 7% пациентов, ненатяжная пластика – у 8% пациентов. Рецидивов ПВГ после выполненной пластики по методикам in-lay и sub-lay выявлено не было.
Мультифакторный сравнительный анализ клинических случаев у пациентов ретроспективной группы с рецидивом ПВГ и без такового позволил выделить факторы риска возникновения рецидива ПВГ. Факторами, оказывающими достоверное влияние на возникновение рецидива ПВГ у больных пожилого и старческого возраста, являются: нагноение операционной раны (вероятность рецидива 35,7%), пластика грыжевого дефекта только местными тканями (вероятность рецидива 29,7%), клинически значимые нарушения функции внешнего дыхания в послеоперационном периоде (вероятность рецидива 12,6%), наличие симптомов недифференцированной дисплазии соединительной ткани (вероятность рецидива 12,6%), а также развитие послеоперационной пневмонии (вероятность рецидива 9,4%).
Ретроспективный анализ позволил заключить, что наилучшими непосредственными и отдаленными результатами при обширных и гигантских ПВГ у пациентов пожилого и старческого возраста характеризуются вмешательства с комбинированным вариантом аутоаллопластики по методикам sub-lay, in-lay. Очевидно, что для предупреждения рецидива ПВГ следует использовать варианты комбинированной аутоаллопластики (sub-lay, on-lay), а при невозможности последней – ненатяжную аллопластику. От пластики дефекта брюшной стенки местными тканями при операциях по поводу ПВГ у пациентов старших возрастных групп следует отказаться.
Отдельной проблемой хирургического лечения пациентов с послеоперационными вентральными грыжами является повышение внутрибрюшного давления (интраабдоминальная гипертензия, ИАГ), возникающая при перемещении содержимого грыжевого мешка в брюшную полость в ходе выполнения пластики брюшной стенки и часто сопровождающаяся клинически значимыми функциональными нарушениями со стороны дыхательной и сердечно-сосудистой систем [4]. Особенно актуально рассмотрение данной проблемы в группе пациентов пожилого и старческого возраста, где ИАГ развивается на фоне уже имеющейся сердечной и легочной патологии. Уровень внутрибрюшного давления, повышение которого приводит к развитию клинически значимой ИАГ, до сих пор остается предметом дискуссии. До середины 1990-х годов доминировало представление о критическом значении ИАГ в 15-18 мм рт.ст. (20-25 мм вод.ст.). В 1996 году Burch была разработана классификация интраабдоминальной гипертензии [6], предусматривающая выделение четырех степеней ИАГ: I степень - 12-15 мм рт.ст., II степень - 16-20 мм рт.ст., III степень - 21-25 мм рт.ст. и IV степень - более 25 мм рт.ст. [4]. Известно, что одномоментное повышение ИАГ до III-IV степени, что имеет место при вправлении содержимого грыжевого мешка в брюшную полость и, тем более, при натяжной пластике грыжевого дефекта, сопровождается трудно контролируемыми и зачастую фатальными нарушениями функционирования сердечно-легочного комплекса.
В этой связи с целью проведения целенаправленной профилактики послеоперационных системных осложнений у пожилых пациентов с ПВГ была разработана методика моделирования этапа вправления содержимого грыжевого мешка («модель вправления») и этапа восстановления целостности мышечно-фасциального комплекса передней брюшной стенки («модель натяжения»). Целью создания данных моделей являлись определение толерантности пациентов к ИАГ и проведение предоперационной адаптации органов брюшной полости и грудной клетки к повышенному внутрибрюшному давлению, возникающему в ходе выполнения грыжесечения и пластики передней брюшной стенки. Методика моделирования условий вправления и натяжения заключалось в следующем. Сразу после проведения первичной спирометрии (измерялись объемы жизненной емкости легких и форсированного выдоха за первую секунду) и измерения внутрибрюшного давления (ВБД) по методике I. Kron (1984), основанной на определении давления в мочевом пузыре, у пациента моделировалась ситуация вправления грыжевого содержимого в брюшную полость (ненатяжная аллопластика); данное положение внутренних органов фиксировалось упругим бандажом в течение 1 часа. Далее проводилось повторное измерение внутрибрюшного давления и второе спирометрическое исследование, которое позволяло выявить толерантность пациента к повышению внутрибрюшного давления и степень увеличения последнего.
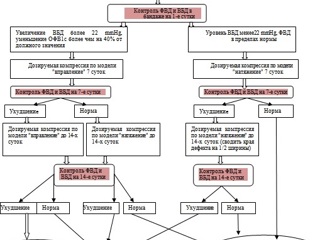
У пациентов, которые перенесли вправление грыжи без критических изменений показателей (объем форсированного выдоха за первую секунду снижается на 40 % и более и повышения ВБД до 22 мм рт ст и выше, производилось сопоставление краев грыжевого дефекта и в течение 1 часа моделировалась ситуация натяжной пластики передней брюшной стенки. На второй день исследования это моделирование натяжения продолжалось в течение 2 часов, с последующей ежедневной прибавкой по 2 часа. Таким образом, к 14-м суткам проведения исследования пациент 24 часа в сутки находился в бандаже. В течение первых 7-ми суток проводились ежедневный контроль уровня ВБД и спирометрия. На 14, 21 и 28-е сутки повторялись тестовые измерения показателей ВБД и спирометрия. При нормальных показателях ВБД и спирометрии этим пациентам выполнялась радикальная комбинированная аутоаллопластика передней брюшной стенки.
Пациентам, у которых было отмечено ухудшение спирометрических параметров на модели вправления, далее проводилась дозируемая контролируемая компрессия брюшной стенки упругим бандажом, цель которой заключалась в постепенной адаптации брюшной полости и легких под ежедневным контролем уровня ВБД и спирометрии. На 2-й день исследования продолжительность модели вправления составила 2 часа с последующей ежедневной прибавкой по 2 часа в сутки до 7 дня. Затем проводилась спирометрия и измерение ВБД (также как и в первом варианте). Если показатели приближались к нормальным, то таким пациентам далее создавалась модель «натяжения» и они впоследствии велись также как и в первом варианте. Пациентам без положительной динамики мы продолжали фиксировать с помощью бандажа "модель вправления", далее проводился контроль ВБД и спирометрия. При удовлетворительных результатах еще в течение 7 суток этим пациентам проводились ежедневные «тренировки» с прибавкой по 2 часа ежедневно и к 14 суткам они также находились в бандаже 24 часа в сутки.
Для оценки практической значимости предложенной методики нами проведена апробация вышеописанных моделей на группе из 31 пациента в возрасте 65 – 84 лет с гигантскими (12 пациентов) и обширными (19 пациентов) послеоперационными вентральными грыжами. Мониторинг внутрибрюшного давления в данной группе пациентов выявил, что в среднем адаптация к абдоминальной компрессии наступает у большинства пациентов к 14-м суткам.
Методика исследования пациентов проспективной группы явилась основой лечебного алгоритма позволяющего аргументировано выбрать тот или иной вариант оперативного вмешательства («ненатяжная» или «натяжная» пластика) на основании определения возможности его проведения, а также подготовить пациента пожилого или старческого возраста с ПВГ обширных и гигантских размеров к операции. При этом возможность вправления грыжи и закрытия грыжевого дефекта с натяжением или без такового, определяется при спирометрии (возникновение критических рестриктивно-обструктивных нарушений) и измерении ВБД во время дозированного бандажирования. Степень компрессии передней брюшной стенки упругим бандажом устанавливается на основании расчета объема грыжевого выпячивания с моделированием его вправления и (или) натяжения краев грыжевого дефекта. В процессе предоперационной подготовки проводится ежедневный мониторинг внутрибрюшного давления и спирометрия.
Апробация представленного лечебного алгоритма проводилась при лечении 78 пациентов пожилого и старческого возраста с большими и гигантскими ПВГ (31 пациент проспективной экспериментальной группы и 47 пациентов проспективной основной группы), из которых у 38% пациентов имели место грыжи гигантских размеров и у 62% пациентов имели место грыжи обширных размеров. При использовании моделей вправления и натяжения было установлено, что поэтапная дозированная абдоминальная компрессия позволила подготовить к ненатяжной пластике всех больных с обширными и гигантскими ПВГ, к натяжной пластике - 89% пациентов. Особенности и результаты лечения больных в основной проспективной группе оказались следующими. Оперативное вмешательство по поводу ПВГ выполнено всем пациентам. Операции в объеме ненатяжной протезирующей пластики выполнены 11% пациентов, натяжная аутоаллопластика выполнена 89% пациентов. Местные осложнения в раннем послеоперационном периоде возникли у 13% пациентов (образование подкожных сером, требующих пункционного дренирования - 10%, нагноение раны - 3%). Системные осложнения возникли у 4% пациентов (ТЭЛА - 2% и послеоперационная пневмония 2%). Количество местных осложнений уменьшилось в 4 раза, а системных в 6 раз по сравнению с пациентами ретроспективной группы. Рецидивов грыжи за двухлетний период наблюдений не выявлено.
Проведенное исследование позволило сделать следующие выводы. Факторами, оказывающими достоверное влияние на возникновение рецидива послеоперационной вентральной грыжи у больных пожилого и старческого возраста являются нагноение операционной раны (вероятность рецидива 35,7%), пластика передней брюшной стенки только местными тканями (вероятность рецидива 29,7%), клинически значимые нарушения функции внешнего дыхания в послеоперационном периоде (вероятность рецидива 12,6%), наличие признаков недифференцированной дисплазии соединительной ткани (вероятность рецидива 12,6%), возникновение послеоперационной пневмонии (вероятность рецидива 9,4%).
Наилучшими отдаленными результатами при обширных и гигантских послеоперационных грыжах характеризуются вмешательства с комбинированным вариантом аутоаллопластики по методикам sub-lay, in-lay (рецидивы отсутствуют).
Разработанные модели вправления и натяжения позволяют до операции прогнозировать изменения внутрибрюшного давления и функции внешнего дыхания у пациента после ненатяжной аллопластики и комбинированной аутоаллоапластики соответственно, а также проводить предоперационную подготовку (адаптацию) пациента к данным вариантам пластики.
Факторами, ограничивающими возможность выполнения комбинированной аутоаллопластики у пациентов старших возрастных групп с обширными и гигантскими послеоперационными вентральными грыжами, являются выявленные при дооперационном моделировании натяжения величина внутрибрюшного давления 22 mmHg и более, а также уменьшение объема форсированного выдоха на 40% от должного значения, не имеющие тенденцию к уменьшению при дозированной поэтапной компрессии брюшной стенки в течение 14 суток.
Применение при лечении пациентов старших возрастных групп с обширными и гигантскими послеоперационными вентральными грыжами алгоритмизированного тактического подхода, основанного на поэтапном моделировании состояния после ненатяжной и натяжной пластики под контролем внутрибрюшного давления и функции внешнего дыхания, позволило выполнить комбинированную аутоаллопластику у 89% пациентов, снизив при этом уровень общесоматических послеоперационных осложнений до 5% и местных послеоперационных осложнений до 13%. Внедрение в клиническую практику данного алгоритмизированного подхода обусловило отсутствие рецидивов послеоперационных вентральных грыж в течение двухлетнего периода наблюдения.
ЛИТЕРАТУРА:
- Белоконев В.И. Пластика брюшной стенки при вентральных грыжах комбинированным способом /В.И. Белоконев, СЮ. Пушкин, З.В. Ковалева //Хирургия.- 2000,- №8.- 24-26.
- Егиев В.Н. Атлас оперативной хирургии грыж /В.Н Егиев, К.В. Лядов, П.К. Воскресенский.- М.,2003.- 228 с.
- Измайлов С.Г., Лазарев В.М., Капустин К.В., Бодров А.А. Лечение послеоперационных вентральных грыж аппаратным способом под контролем внутрибрюшного давления. Вестник герниологии, 2004. М. С. 52-59.
- Курбонов К.М. Абдоминальный компартмент-синдром в хирургии послеоперационных грыж живота /К.М. Курбонов гигантских //Герниология.- 2004.- №3.- 28-29.
- Жебровский В.В. Хирургия грыж живота. – М.: ООО «Медицинское информационное агентство», 2005; с. 296-360.
- Burch J.M., Moore E.E., Moore F.A., Franciose R . The abdominal compartment syndrome // Surg Clin North Am 1996 Aug; 76 (4): P. 833 – 842.
7 мая 2016 г.
Ещё больше полезной информации на нашем Телеграм-канале